Niebieski
Gdy pies nasika chemikowi na ścianę...
Pittakall to prawdopodobnie pierwszy syntetyczny barwnik organiczny*, jaki pojawił się w handlu, choć nie zdobył zbyt dużej popularności i dość szybko zarzucono jego produkcję. Jego przypadkowym odkrywcą był niemiecki chemik Karl Reichenbach. Na początku XIX wieku zarządzając małą fabryką chemiczną zajął się badaniem produktów suchej destylacji drewna, węgla i szczątków organicznych. To on wydzielił ze smoły różne wartościowe frakcje, w tym kreozot, parafinę czy fenol, a także pierwszy olej opałowy nazwany eupinonem.
Kreozot, będący frakcją smoły z drewna drzew liściastych, miał dość charakterystyczną, silną woń oraz dobre właściwości konserwujące, dlatego chemik zaczął stosować go do impregnowania drewna. Do dziś zresztą jest częstym składnikiem impregnatów, na przykład do podkładów kolejowych.
Postanowił wypróbować go także w zastosowaniu dużo bardziej przyziemnym - przeszkadzało mu, że psy sikają mu zewnętrzną ścianę domu, więc posmarował ją kreozotem aby zapach je odstraszał. Psom najwyraźniej było wszystko jedno, bardzo lubiły tam stawać i podnosić nogę, lejąc bezczelnie po wysmarowanej ścianie. Cóż, widocznie nie było to dobry środek na psy.
Przyglądając się ich działalności zauważył jednak ciekawą rzecz - w miejscu gdzie stały plamy moczu, na ziemi pojawiło się wyraźne, niebieskie zabarwienie. A ponieważ był człowiekiem bardzo praktycznym, zaczął czynić próby powtórzenia reakcji. Szybko wykrył, że mocz nie jest w jej potrzebny, stanowił jedynie alkaliczny reagent. Prowadząc destylację surowej smoły stwierdził, że frakcja o temperaturze wrzenia wyższej niż kreozot, po wprowadzeniu do wody wapiennej lub roztworu wodorotlenku baru, po pewnym czasie zamienia się w ciemnogranatowy proszek.
Wprowadził go na rynek jako pigment nadający się do farbowania po rozpuszczeniu w alkaliach. Najwyraźniej jednak nie miał zbyt dobrych właściwości i po pewnym czasie przestał być używany, pojawiając się jedynie od czasu do czasu w historycznych spisach barwników. Dopiero pod koniec XIX wieku ustalono, że jest to związek będący produktem kondensacji pirogallolu, o strukturze podobnej do barwników trifenylometylenowych. W formie anionowej przybierał intensywny kolor. Pigment Reichenbacha był laką, to jest nierozpuszczalną solą barową lub wapniową.
Pittakall jest dziś w zasadzie historyczną ciekawostką. Mam wrażenie, że od ponad stu lat nikt go nie otrzymywał, bo poza wzmiankami w pracach o historii barwników nie znalazłem o nim żadnej dalszej informacji ani tym bardziej zdjęcia próbki. Ponoć miał dość ciemny odcień niebieskiego.[1]
Ftalocyjanina
Kolejny niebieski barwnik także został odkryty niezamierzenie, podczas otrzymywania czegoś innego, i to dwa razy.
W 1927 roku szwajcarscy chemicy Henri Diesbach i Edmond von de Weid zajmowali się znalezieniem lepszej niż już znane metody otrzymywania ftalonitrylu, to jest pochodnej benzenu z dwiema grupami -CN. Znana była już w tym czasie reakcja Sandmeyera, polegająca na podstawieniu soli diazoniowych, gdzie grupa -NN była łatwo zamieniana na inne. Przy jej pomocy otrzymywano ftalonitryl z o-aminobenzonitrylu (a ten z rozkładu termicznego amidu kwasu antranilowego).
Badacze postanowili spróbować nieco innej metody, której substrat był bardziej stabilny i łatwiejszy w otrzymaniu. Była to reakcja Rosenmunda-von Brauna (nie mylić z reakcją Rosenmunda samego, czyli redukcją kwasów do aldehydów) polegająca na podstawieniu halogenku przy pierścieniu aromatycznym, przez anion cyjankowy z cyjanku miedzi.[2]
Jako substratu użyli 1,2-dibromobenzenu. Pomysł był w istocie dosyć prosty, reakcja powinna przebiegać w taki oto sposób:
Produktem powinna być bezbarwna lub nieco żółtawa krystaliczna substancja. Jakież więc było zdziwienie chemików, gdy po reakcji znaleźli w kolbie osad intensywnie niebieski.
Produkt był bardzo trwały, nierozpuszczalny w wodzie i dość trudno w innych rozpuszczalnikach. Po wyznaczeniu przez analizę elementarną składu C26H18N6Cu uznali, że prawdopodobnie mają do czynienia ze związkiem kompleksowym ftalonitrylu i pirydyny, zawierającym jeden atom miedzi i po dwie cząsteczki tych związków [3]. Ale mylili się.
Drugimi odkrywcami byli chemicy w fabryce Scottish Dyes (dziś ICI), którzy w 1928 roku analizowali metodę przemysłowego otrzymywania ftalimidu. Bezwodnik ftalowy był w tej syntezie poddawany reakcji z amoniakiem w stężonym roztworze wodnym, zaś jako reaktorów używano emaliowanych żeliwnych kotłów. Mechaniczne mieszadło powodowało, że emalia z czasem się zdzierała, zaś pilnujący procesu technolodzy zauważyli, że partie produktu z tych najbardziej wytartych kotłów były zanieczyszczone drobnym, niebieskawym osadem. Było zresztą zauważalne, że na niebieskawy kolor zabarwił się odsłonięty metal.
Po zebraniu większej ilości zanieczyszczenia, pracownicy fabryki zdali sobie sprawę z tego, że potencjalnie mógłby to być niezły pigment, miał bowiem niską rozpuszczalność i bardzo dużą siłę barwiącą. Kolejną więc syntezę przeprowadzono dodając do masy wiórki żelazne, był to jednak proces mało wydajny. Należało odpowiedzieć na pytanie, co właściwie zachodzi w reaktorze i jaki związek otrzymano.
Po wpływem silnych alkaliów związek tracił metal, powstała wolna forma nadal była niebieska ale o dużo słabszym odcieniu. Można było połączyć ją z innymi metalami, zwłaszcza ze szczególnie chętnie wiązaną miedzią, tworząc kompleksy bardzo trwałe i intensywnie zabarwione. Analizy pokazały, że związek ma charakter aromatyczny i być może zawiera układ skumulowanych pierścieni. Dopiero w 1933 roku Patrick Linstead zaproponował dla związku budowę makrocykliczną, podobną do porfiryny, z czterema fragmentami benzopirolu połączonymi przez mostkowe azoty, co potwierdziły potem badania rentgenowskie.
Firma ICI zaczęła produkować pigment w 1934 roku po udoskonaleniu metod pod nazwą Monastral Blue, lub błękit ftalocyjaninowy. Był wielkim osiągnięciem. Niebieskich pigmentów było w tym czasie niewiele, w zasadzie istniały tylko nieorganiczne oparte o sole miedzi i ultramarynę, oraz indygo i jego pochodne. Błękit ftalocyjaninowy miał tą zaletę, że będąc barwnikiem organicznym posiadał wysoką odporność na blaknięcie, miał dużą siłę barwiącą, był na tyle słabo rozpuszczalny że nie migrował do innych warstw malarskich, oraz był dosyć odporny na czynniki fizyczne i chemiczne. Związek ten rozkłada się dopiero w temperaturze 600 stopni.
Do dziś jest jednym z najczęściej wykorzystywanych barwników, zwłaszcza do farb do metalu, ale też atramentów czy tuszu do długopisów. Jest na przykład składnikiem standardowego tuszu niebieskiego do drukarek, a ze względu na znikomą toksyczność także pigmentów do tatuażu.
Niezamierzony niebieski pigment
To odkrycie także miało pewien element przypadkowości.
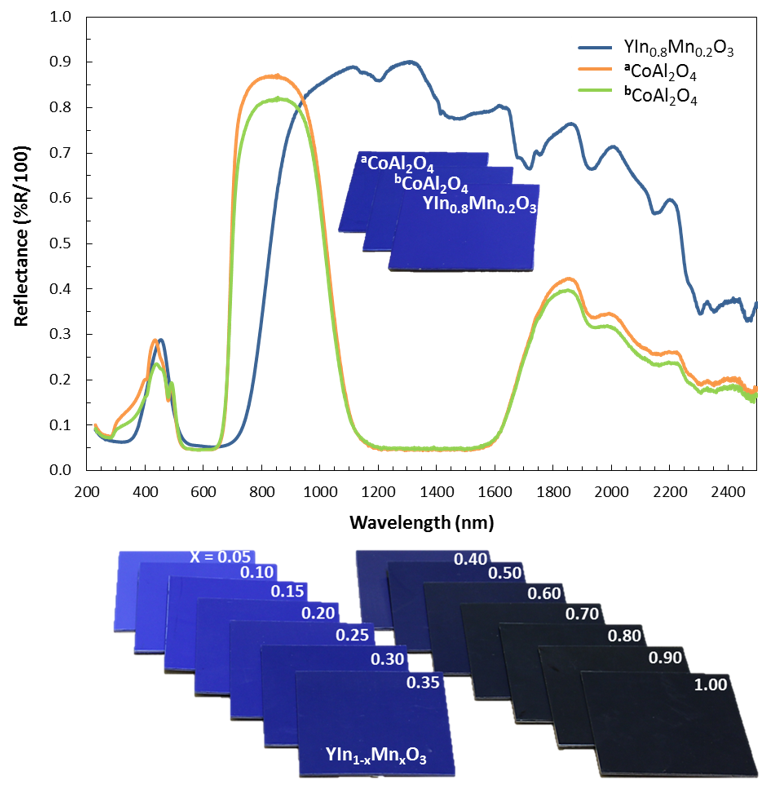
Zespół profesora Subramaniana, na uniwersytecie stanowym w Oregonie, zajmował się badaniami tlenkowych materiałów ceramicznych z solami ziem rzadkich, które mogłyby potencjalnie znaleźć zastosowanie w elektronice. Niektóre mogłyby okazać się magnesami stałymi, inne nadprzewodnikami niskotemperaturowymi, ferroelektrykami czy superopornikami. Studenci profesora biorący udział w pracach testowali więc różne mieszanki tlenków i chlorków metali, które po wymieszaniu w młynie kulowym na bardzo drobny proszek wypalano w odpowiedniej temperaturze.
Doktorant Andrew E. Smith spróbował pewnego razu nietypowej mieszanki tlenku itru, indu i manganu VI. Dwutlenek manganu jest intensywnie czarny, dlatego po zmieleniu uzyskał ciemnoszary proszek. Następnie wsadził go na chwilkę do pieca aby się wygrzał. Temperatura szybko osiągnęła prawie 1100 stopni, a tlenki przereagowały ze sobą, tworząc nowe połączenie. Akurat to konkretne nie miało szczególnie ciekawych własności elektrycznych czy magnetycznych, lecz jedna właściwość rzucała się w oczy od razu po wyjęciu z pieca - otrzymany proszek okazał się niesamowicie niebieski.[4]
Gdy profesor zobaczył próbkę od razu przyszło mu do głowy, że to może znaleźć zastosowanie. Właściwie jeszcze przed publikacją na temat związku zaczęto starania nad komercjalizacją.
Jak się okazało podczas wyprażania powstaje związek zawierający warstwy tlenku manganu o nietypowej koordynacji w formie bipiramidy trygonalnej. W każdej takiej jednostce atom manganu otoczony jest przez pięć atomów tlenu, w tym trzy w płaszczyźnie warstwy i po jednym nad i pod nią. W takim położeniu oddziaływanie ligandów powoduje rozszczepienie poziomów energetycznych orbitali d manganu w taki sposób, że związek pochłania światło czerwone i zielone dając w efekcie niebieski kolor.
Wcześniej znany był pigment oparty o manganian baru, ale miał małą stabilność, nowy pigment nazwany YInMn nie tylko jest odporny na utlenienie czy redukcję, ale też zachowuje kolor w bardzo wysokich temperaturach i nie blaknie pod wpływem wilgoci. Szybko okazało się, że dobrze nadaje się zarówno do farb olejowych jak i wodnych, a także jako pigment do barwienia mas plastycznych. W tych zastosowaniach ważną własnością jest też jego nietoksyczność. Inne pigmenty nieorganiczne podobnej trwałości zwykle zawierają sole rakotwórczego kobaltu lub sole miedzi.
Podczas dalszych badań stwierdzono, że choć związek silnie pochłania światło czerwone, to zarazem silnie odbija podczerwień, osiągając jeden z najwyższych współczynników odbicia dla materiałów niemetalicznych (srebro odbija niemal 100% podczerwieni). Dzięki temu powierzchnie pomalowane farbą z tym pigmentem bardzo mało się nagrzewają, co miałoby znaczenie w przypadku na przykład dachów w cieplejszych krajach
Obecnie pigment zaczyna powoli wchodzić na rynek, niedawno producent kredek świecowych i pasteli Crayola ogłosił wprowadzenie kredki z YInMn, trwa konkurs na wymyślenie nazwy [5].
Jednak wbrew temu co piszą media, pigment nie posiada nowego, dopiero teraz odkrytego odcienia niebieskiego. W najbardziej optymalnym składzie YIn0.8Mn0.2O3 , związek ma kolor błękitu kobaltowego lub nieco cieplejszy, mimo zupełnie różnego przebiegu krzywej absorpcji:
Odcień może płynnie zmieniać się w zależności od stosunku itru do manganu. Dodatek innych metali, na przykład tytanu czy cynku może natomiast zmienić kolor na zielony lub fioletowy.[6]
W zespole prof. Subramaniana trwają prace nad uzyskaniem pigmentu czerwonego o odcieniu i intensywności nie stosowanych dziś z powodu toksyczności pigmentów rtęciowych jak cynober.
Może jeszcze kiedyś napiszę coś o projektowaniu barwników aby pokazać, jak takie rzeczy otrzymuje się planowo, bez czekania na szczęśliwy przypadek.
-------
* Aczkolwiek wcześniej niż Pittakall bo w XVIII wieku stworzono kwas pikrynowy, przez pewien czas używany do farbowania wełny, zastosowanie jako barwnik znalazł jednak dużo później. Półsyntetyczny był natomiast otrzymany w podobnym czasie indygokarmin, znany jako błękit saksoński, pozyskiwany przez traktowanie indygo dymiącym kwasem siarkowym.
[1] George B. Kauffman, Pittacal - The first synthetic dyestuff, Journal of Chemical Education (12) 1977 str. 753
[2] Sandmeyer-von Braun reaction
[3] De Diesbach, Henri; von Der Weid, Edmond (1927). "Quelques sels complexes des o-dinitriles avec le cuivre et la pyridine". Helvetica Chimica Acta. 10: 886.
[4] http://oregonstate.edu/ua/ncs/archives/2009/nov/accidental-discovery-produces-durable-new-blue-pigment-multiple-applications-0
[5] http://oregonstate.edu/ua/ncs/archives/2017/may/pigment-discovered-oregon-state-university-inspires-new-crayola-crayon-color
[6] http://chemistry.oregonstate.edu/content/story-yinmn-blue
informacje
piątek, 19 maja 2017
wtorek, 2 maja 2017
Stabilny zwiazek helu?
W artykule na temat związków chemicznych gazów szlachetnych (link) opisałem kilka przypadków w których teoretycznie niereaktywne pierwiastki są jednak w stanie utworzyć połączenia. Helowce ciężkie, jak krypton czy ksenon tworzą wiele związków, co ułatwia stosunkowo niska jak na tą grupę energia jonizacji. Jednak im bardziej w górę, tym z tym gorzej - energia jonizacji rośnie a już dla helu tworzenie wiązań kowalencyjnych uniemożliwiają pewne efekty związane z zapełnianiem orbitali.
Najnowsze odkrycie opublikowane właśnie w The Nature pokazuje jednak, że nie jest to zastrzeżenie tak ścisłe. Wprawdzie otrzymane kryształy helu z sodem nie są klasycznym połączeniem chemicznym, ale mają zdefiniowaną strukturę i stały skład, oraz pokazują coś, czego dotąd o własnościach helu nie wiedzieliśmy.
Mieszanina helu i metalicznego sodu pod ciśnieniem ponad 100 gigapaskali utworzyła szczególną strukturę, nazywaną elektrydem. Jest to w pewnym sensie sól elektronów - swobodny elektron zawarty w lukach struktury odgrywa rolę bardzo małego anionu, związanego z kationami metalu wokół.
Dość stabilne elektrydy są znane dla związków krystalizowanych z roztworów zawierających solwatowane elektrony, na przykład roztworów metali alkalicznych w amoniaku czy kryptandach, otrzymano też elektryd stabilny w temperaturze pokojowej, w której elektron został zamknięty w klatkowatej strukturze glinianu wapnia podobnej do zeolitów.
Niedawno stwierdzono powstawanie elektrydów także w metalach alkalicznych pod skrajnie wysokim ciśnieniem. Zewnętrzny nacisk powoduje, że atomy metalu są dociskane do siebie. Ze względu na odpychanie oraz konieczność spełniania reguły Pauliego, powłoki elektronowe są deformowane. Najwidoczniej dobrym sposobem na ustabilizowanie i zmniejszenie odpychania jest w tej sytuacji utworzenie struktury jonowej, z małymi wnękami zawierającymi zamknięte elektrony jako aniony i zawarte w sieci kationy metalu.
Możliwość tworzenia takich struktur zainteresowała zespół rosyjskich badaczy pod kierunkiem A. R. Oganowa. Na podstawie symulacji stwierdził on, że dla wysokich ciśnień powinno być możliwe utworzenie dość luźnej struktury zawierającej we wnękach także hel. Po długich przygotowaniach przetestowano tą możliwość stwierdzając, że po zastosowaniu przewidzianego ciśnienie połączenie takie powstaje dość łatwo.
Jak jednak wygląda ta struktura i jaka jest w niej rola helu?
Zasadniczo atomy sodu tworzą prostą sieć regularną, w której tworzą układ stykających się kostek z atomami w narożach, na powyższej wizualizacji są to fioletowe kulki. Wewnątrz jednych z tak powstałych luk znajdują się atomy helu nie oddziałujące z atomami sodu (zielone kostki), a wewnątrz innych tworzące anion dwa elektrony. Oddziałują one z sodem, przez co na mapach gęstości przyjmują formę ośmiościanów (tu czerwone okaedry we wnękach).
Wśród propozycji opisu sposobu w jaki niezwiązane elektrony oddziałują ze strukturą pojawia się wiązanie ośmiocentrowe-dwuelektronowe, jednak jest to dość pokrętna propozycja.
Tak powstałe połączenie jest trwałe tylko pod wysokim ciśnieniem.
Związek?
Atomy helu są w tej strukturze wprawdzie zawarte, ale nie tworzą żadnych wiązań, nie są więc ani składnikiem kowalencyjnym, ani jonowym. W pewnym sensie stanowią neutralną przekładkę stabilizującą strukturę. Bez nich układ atomów sodu byłby zbyt luźny, puste kostki nie powstrzymywałyby atomów przed zapadaniem w bardziej ścisłe człony. Można by je było oczywiście wypełnić następnymi parami elektronów, ale wtedy układ czterech kationów mógłby nie tworzyć regularnych klatek ze względu na wzajemne odpychanie. W zasadzie więc bez helu taka struktura by nie powstała.
Znane są już połączenia klatkowe, gdzie atomy helu są obecne w lukach innego materiału, na przykład klatraty czy pewna odmiana krystobalitu. Udało się też stworzyć hel zamknięty w fullerenach, z których nie jest w stanie się uwolnić, choć z nimi chemicznie nie oddziałuje. W tym przypadku połączenie elektrydowe z sodem wydaje się bardzo podobne, lecz rola atomów w strukturze jest nieco bardziej skomplikowana. Czy zatem jest to jakiś dziwny związek? To już zależy jak sobie związki zdefiniujemy.
Nietypowa struktura, niewiele wysokociśnieniowych aparatur zdolnych powtórzyć eksperyment, i dośc pokrętny opis teoretyczny spowodowała, że artykuł o odkryciu ukazał się dopiero po ponad dwóch latach, recenzenci chcieli być bowiem pewni, że nie jest to jakaś pomyłka.
Obecnie zespół badawczy pracuje nad otrzymaniem innych takich struktur. Wedle symulacji dodanie do mieszaniny atomów tlenu obniża ciśnienie potrzebne do stworzenie elektrydu dziesięciokrotnie.
--------
* X. Dong, A.R. Oganov, A.F. Goncharov, E. Stavrou, S. Lobanov, G. Saleh, G. Qian, Q. Zhu, C. Gatti, V.L. Deringer, R. Dronskowski, X. Zhou, V.B. Prakapenka, Z. Konôpková, I.A. Popov, A.I. Boldyrev, and H. Wang, "A stable compound of helium and sodium at high pressure", Nature Chemistry, 2017. http://dx.doi.org/10.1038/nchem.2716
* https://en.wikipedia.org/wiki/Helium_compounds
Najnowsze odkrycie opublikowane właśnie w The Nature pokazuje jednak, że nie jest to zastrzeżenie tak ścisłe. Wprawdzie otrzymane kryształy helu z sodem nie są klasycznym połączeniem chemicznym, ale mają zdefiniowaną strukturę i stały skład, oraz pokazują coś, czego dotąd o własnościach helu nie wiedzieliśmy.
Mieszanina helu i metalicznego sodu pod ciśnieniem ponad 100 gigapaskali utworzyła szczególną strukturę, nazywaną elektrydem. Jest to w pewnym sensie sól elektronów - swobodny elektron zawarty w lukach struktury odgrywa rolę bardzo małego anionu, związanego z kationami metalu wokół.
Dość stabilne elektrydy są znane dla związków krystalizowanych z roztworów zawierających solwatowane elektrony, na przykład roztworów metali alkalicznych w amoniaku czy kryptandach, otrzymano też elektryd stabilny w temperaturze pokojowej, w której elektron został zamknięty w klatkowatej strukturze glinianu wapnia podobnej do zeolitów.
Niedawno stwierdzono powstawanie elektrydów także w metalach alkalicznych pod skrajnie wysokim ciśnieniem. Zewnętrzny nacisk powoduje, że atomy metalu są dociskane do siebie. Ze względu na odpychanie oraz konieczność spełniania reguły Pauliego, powłoki elektronowe są deformowane. Najwidoczniej dobrym sposobem na ustabilizowanie i zmniejszenie odpychania jest w tej sytuacji utworzenie struktury jonowej, z małymi wnękami zawierającymi zamknięte elektrony jako aniony i zawarte w sieci kationy metalu.
Możliwość tworzenia takich struktur zainteresowała zespół rosyjskich badaczy pod kierunkiem A. R. Oganowa. Na podstawie symulacji stwierdził on, że dla wysokich ciśnień powinno być możliwe utworzenie dość luźnej struktury zawierającej we wnękach także hel. Po długich przygotowaniach przetestowano tą możliwość stwierdzając, że po zastosowaniu przewidzianego ciśnienie połączenie takie powstaje dość łatwo.
Jak jednak wygląda ta struktura i jaka jest w niej rola helu?
Zasadniczo atomy sodu tworzą prostą sieć regularną, w której tworzą układ stykających się kostek z atomami w narożach, na powyższej wizualizacji są to fioletowe kulki. Wewnątrz jednych z tak powstałych luk znajdują się atomy helu nie oddziałujące z atomami sodu (zielone kostki), a wewnątrz innych tworzące anion dwa elektrony. Oddziałują one z sodem, przez co na mapach gęstości przyjmują formę ośmiościanów (tu czerwone okaedry we wnękach).
Wśród propozycji opisu sposobu w jaki niezwiązane elektrony oddziałują ze strukturą pojawia się wiązanie ośmiocentrowe-dwuelektronowe, jednak jest to dość pokrętna propozycja.
Tak powstałe połączenie jest trwałe tylko pod wysokim ciśnieniem.
Związek?
Atomy helu są w tej strukturze wprawdzie zawarte, ale nie tworzą żadnych wiązań, nie są więc ani składnikiem kowalencyjnym, ani jonowym. W pewnym sensie stanowią neutralną przekładkę stabilizującą strukturę. Bez nich układ atomów sodu byłby zbyt luźny, puste kostki nie powstrzymywałyby atomów przed zapadaniem w bardziej ścisłe człony. Można by je było oczywiście wypełnić następnymi parami elektronów, ale wtedy układ czterech kationów mógłby nie tworzyć regularnych klatek ze względu na wzajemne odpychanie. W zasadzie więc bez helu taka struktura by nie powstała.
Znane są już połączenia klatkowe, gdzie atomy helu są obecne w lukach innego materiału, na przykład klatraty czy pewna odmiana krystobalitu. Udało się też stworzyć hel zamknięty w fullerenach, z których nie jest w stanie się uwolnić, choć z nimi chemicznie nie oddziałuje. W tym przypadku połączenie elektrydowe z sodem wydaje się bardzo podobne, lecz rola atomów w strukturze jest nieco bardziej skomplikowana. Czy zatem jest to jakiś dziwny związek? To już zależy jak sobie związki zdefiniujemy.
Nietypowa struktura, niewiele wysokociśnieniowych aparatur zdolnych powtórzyć eksperyment, i dośc pokrętny opis teoretyczny spowodowała, że artykuł o odkryciu ukazał się dopiero po ponad dwóch latach, recenzenci chcieli być bowiem pewni, że nie jest to jakaś pomyłka.
Obecnie zespół badawczy pracuje nad otrzymaniem innych takich struktur. Wedle symulacji dodanie do mieszaniny atomów tlenu obniża ciśnienie potrzebne do stworzenie elektrydu dziesięciokrotnie.
--------
* X. Dong, A.R. Oganov, A.F. Goncharov, E. Stavrou, S. Lobanov, G. Saleh, G. Qian, Q. Zhu, C. Gatti, V.L. Deringer, R. Dronskowski, X. Zhou, V.B. Prakapenka, Z. Konôpková, I.A. Popov, A.I. Boldyrev, and H. Wang, "A stable compound of helium and sodium at high pressure", Nature Chemistry, 2017. http://dx.doi.org/10.1038/nchem.2716
* https://en.wikipedia.org/wiki/Helium_compounds
poniedziałek, 24 kwietnia 2017
Chemiczne wieści (10.)
Aldehydy w elektronicznych papierosach
Elektroniczne papierosy pojawiły się na rynku stosunkowo niedawno, i wciąż nie do końca znane są ich skutki zdrowotne. Na pewno, ze względu na brak substancji smolistych, nie są tak bardzo szkodliwe jak papierosy tytoniowe, jednak badań długotrwałego wpływu jest generalnie niewiele.
Chemicy wskazują, że skład mgiełki produkowanej przez te urządzenia, nie jest tak zupełnie bezpieczny, jak to się mogło wydawać.
Głównym składnikiem liquidów będących wkładem, jest gliceryna lub glikol propylenowy. Związki te są nieszkodliwe. Jednak podczas ich odparowywania na grzałce mogą zachodzić dodatkowe reakcje, prowadzące do powstawania reaktywnych aldehydów, głównie akroleiny, aldehydu mrówkowego i acetaldehydu. Wdychanie ich może zwiększać ryzyko chorób serca i układu krwionośnego. Dotychczasowe badania wskazywały, że mgiełka elektronicznych papierosów zawiera pewną niewielką ilość aldehydów, co jednak trudno było ocenić z powodu z powodu nietrwałości tych związków. Czasem pojawiały się pojedyncze badania wskazujące na wysokie stężenia, być może związane z niewłaściwą techniką poboru próbek (za wolne zaciąganie lub za duże grzanie).
W nowych badaniach mgiełkę wytwarzaną przez dostępne na rynku urządzenia pochłaniano na podłożu z krzemionki pokrytej cząsteczkami alkilowej pochodnej hydroksyloaminy. Ta reagowała z aldehydami tworząc charakterystyczne oksymy, które są dużo trwalsze, dzięki czemu w dalszych analizach łatwiej było odtworzyć rzeczywiste stężenie aldehydów i sprawdzić od jakiś czynników zależy.
Okazało się, że urządzenia nowsze wytwarzają większe stężenia aldehydów niż starsze. Efekt ten był związany z mocniejszymi bateriami i mocniejszymi grzałkami; między mocą grzałki a aldehydami istniała wyraźna zależność. Pewien wpływ miał też czas zaciągania powietrza.
W dodatkowym badaniu przy pomocy techniki NMR sprawdzono powstawanie hemiacetali, mogących ukrywać faktyczne stężenia aldehydów. W przypadku jednego liquidu smakowego wykryto hemiacetale, ale bez przekroczenia bezpiecznych norm, u pozostałych badanych smakowych i bezsmakowych taka reakcja nie zachodziła.
W ostatecznym rozrachunku poziomy aldehydów w aerozolu z e-papierosów są dużo niższe niż w dymie papierosowym (z wyjątkiem przypadków tzw. "suchego zaciągu"), niemniej fakt że jednak w nim występują, oznacza że nie jest to używka dla zdrowia całkiem obojętna.[1]
Spolaryzowana fluorescencja
Fluorescencja to szybki proces w wyniku którego wzbudzone cząsteczki lub atomy wypromieniowują energię w postaci światła. Najbardziej znanym jest świecenie pod wpływem ultrafioletu, wykorzystywane w wybielaczach optycznych. Teraz przedstawiono nietypową tego procesu modyfikację - fluorescencję świecącą od razu światłem spolaryzowanym.
Czynnikiem świecącym były jony rzadkiego pierwiastka europu. Jego sól została rozpuszczona w cieczy jonowej, to jest płynnym związku złożonym tylko z jonów (w zasadzie są to ciekłe sole), w tym przypadku był to kation tetrabutyloamoniowy i anion proliny. Po naświetleniu ultrafioletem roztwór świecił światłem spolaryzowanym kołowo. Kierunek obrotu polaryzacji zależał od tego czy użyta prolina była prawoskrętna czy lewoskrętna. [2]
Ładna demonstracja równowag chemicznych
Czasopismo Journal of Chemical Education mogłoby być w zasadzie zaliczone do pedagogicznych, poświęcone jest bowiem nauczaniu chemii, jednak robi to w ciekawy sposób - większość artykułów to nie biadolenie nad poziomem nauczania, tylko bardzo konkretne propozycje co takiego można uczniom pokazać, aby lepiej wyjaśnić im daną kwestię. Dlatego w zasadzie jest to skarbnica propozycji doświadczeń. W jednym z ostatnich numerów najbardziej wizualnie spodobał mi się artykuł na temat pokazywania równowag kwasowo-zasadowych.
Do czterech próbówek z wodą wsypano kationit kwasowy - to jest granulki specjalnego polimeru, mającego na powierzchni reszty kwasu siarkowego, skłonne oddawać protony. W zasadzie trzeba o nim myśleć jak o kwasie siarkowym osadzonym w plastiku. Do wody dodano odczynnik kwasowo-zasadowy błękit tymolowy. W warunkach obojętnych przybiera kolor żółty. Wprawdzie na dnie znajduje się polimer o właściwościach kwasowych, ale wcale nie oddaje on swoich protonów tak chętnie, musi je podmienić na jakieś inne kationy. Do jednej z próbówek dodajemy więc roztwór soli kuchennej i po chwili obserwujemy jak od dna rozwija się coraz wyraźniejsza różowa barwa, świadcząca o warunkach silnie kwaśnych. Do drugiej dodajemy niedużą ilość roztworu wodorotlenku sodu - w alkalicznym środowisku odczynnik zmienia kolor na błękitny. Jednak wodorotlenek zawiera też kationy sodowe, które mogą podmienić protony w kationicie. Dlatego od dna roztwór zaczyna się zabarwiać na żółto, świadcząc o zakwaszeniu roztworu, a w warstwach najbliżej dna na różowo. Mamy więc roztwór z trzema kolorami - różowym na dole, żółtym powyżej i błękitnym u góry.
| Kolorowa równowaga. Udostępnione przez ACS Publications. |
Co ma tłumaczyć doświadczenie? W próbówce pojawiają się nam dwie równowagi - jedna to równowaga odłączania protonów od kationitu, zależna od stężenia kationów metali w roztworze. Druga to równowaga między trzema różnobarwnymi formami odczynnika, zależna od odczynu. Wreszcie przesuwająca się od dna granica między kolorami ukazuje naocznie szybkość dyfuzji jonów hydroniowych. Po pewnym czasie cały roztwór stanie się różowo-żółty ale wtedy można dodać wodorotlenku jeszcze raz, powtarzając cykl; dla zaproponowanej ilości substratów można tak zrobić do siedmiu razy.
Takie rzeczy powinni pokazywać w szkołach, a nie tylko kreda i tablica. [3]
--------
[1] Mumiye A. Ogunwale et al. Aldehyde Detection in Electronic Cigarette Aerosols, ACS Omega (2017). DOI: 10.1021/acsomega.6b00489
[2] Ben Zercher and Todd A. Hopkins, Induction of Circularly Polarized Luminescence from Europium by Amino Acid Based Ionic Liquids, Inorg. Chem., 2016, 55 (21), pp 10899–10906
[3] Ingo Eilks and Ozcan Gulacar, A Colorful Demonstration to Visualize and Inquire into Essential Elements of Chemical Equilibrium, J. Chem. Educ., 2016, 93 (11), pp 1904–1907
sobota, 15 kwietnia 2017
Jak od-gotować jajko?
Ugotowanie jaja na twardo wydaje się najprostszym i najbardziej prozaicznym procesem kuchennym. Staje się on dużo ciekawszy jeśli spojrzeć nań okiem chemika, który wie jak można ten proces przyspieszyć, a nawet odwrócić.
Jajo to jedna z faz rozwoju ptaków i gadów, w której niedojrzały zarodek zostaje wydalony poza organizm matki w otoczce odżywczego białka i tłuszczu zabezpieczonych twardą, nieprzenikalną skorupką. Jest także jednym z podstawowych produktów spożywczych.
Centralnie położone żółtko, będące głównym materiałem zapasowym rosnącego zarodka, zawiera więcej białek niż wodnisty płyn wokół nazywany białkiem. Jego żółty kolor to zasługa karotenoidów z karmy zjadanej przez kurę, głownie luteiny i zeaksantyny, dlatego odcień może różnić się zależnie od fermy i sposobu chowu, niekiedy gdy w karmie zawarta jest papryka, żółtko może wydawać się wręcz czerwone. Zawiera też tłuszcz zasobny w nienasycone kwasy tłuszczowe i znaczną ilość lecytyny będącej emulgatorem.
Pośrodku jaja utrzymują je elastyczne pasy chelazy.
Większość objętości jaja wypełnia wodniste białko zawierające, jak nazwa wskazuje, dużą ilość białek. Są to głównie albuminy, owotransferryna która kompleksuje żelazo, hamując wzrost bakterii, lizozym który niszczy bakterie Gram dodatnie, czy zapobiegająca przedwczesnemu ścinaniu owomucyna, będąca też głównym alergenem jaj.
Całość utrzymywana w szczelnej białkowej błonce, na którą organizm kury osadził twardą skorupkę zawierającą głównie węglan wapnia. Jej kolor zależy tylko od odmiany kury, w dużym stopniu też od upierzenia - lubiane na Zachodzie białe jajka znoszą głównie odmiany kur biało upierzonych, bardziej popularne u nas jasnobrązowe jaja składają głównie odmiany kur nakrapianych i brązowych, niektóre rasy dają jaja oliwkowe, nawet zielonkawe, albo ciemnobrązowe, z dodatkowymi kropkami.
Denaturacja
Proces ścinania, to jest zamiany formy białek z rozpuszczalnej w stałą, nazywany denaturacją. Może następować pod wpływem czynników fizycznych, a więc zmian temperatury, mechanicznego wytrząsania, naświetlania itp. ale też chemicznych jak jony metali ciężkich, mocne kwasy czy nawet wysokie stężenie soli.
W trakcie tego procesu następuje zmiana ukształtowania nici białkowej. Zwykle przybiera ona w naturze pewien określony kształt wymuszany przez oddziaływania aminokwasów, wiązania wodorowe czy mostki siarczkowe. Utrata tego pierwotnego kształtu zmienia właściwości białka, które może przestać pełnić swoją funkcję, na przykład enzymy stają się nieczynne katalitycznie. Jeśli zmiany te są odwracalne, a po użyciu korzystnych warunków (np. rozcieńczenie stężonego roztworu soli) białko wraca do poprzedniej formy, mówimy o denaturyzacji odwracalnej. Ale często dochodzi też do denaturyzacji nieodwracalnej, po której białko nawet w sprzyjających warunkach nie powróci do poprzedniej formy i funkcji. Enzymy usmażonego mięsa nie będą działać, a gumowata masa jajecznicy nie rozpłynie się po ochłodzeniu czy wymoczeniu w wodzie.
W kurzym jajku głównymi białkami wodnistej części są albuminy, zaliczane do globin, których cząsteczki mają kształt z grubsza kulisty, z hydrofobowymi częściami w środku. Z tego zresztą powodu rozpuszczają się w wodzie tworząc koloidy. Przy bliższym spojrzeniu ich cząsteczki wyglądają podobnie do luźnego kłębka wełny, którym niedawno bawił się kot.
Co jednak ważniejsze, w ich składzie dość często pojawia się siarka. Najczęściej jest to aminokwas cysteina. Jest to ważne, bowiem między dwoma atomami siarki w tej samej cząsteczce lubią się tworzyć mostki dwusiarczkowe, to jest wiązania -S-S-. Ich zaistnienie zmusza łańcuch aminokwasowy do zagięcia a więc w dużym stopniu decyduje o kształcie cząsteczki. Albuminy mogą zawierać kilka takich mostków, tworzących dość stabilną strukturę.
Sieciowanie
Co takiego następuje podczas gotowania? Duże drgania termiczne mają na tyle dużą energię, że mostki dwusiarczkowe ulegają zrywaniu, pękają wiązania wodorowe, zaś nić rozplątuje się i częściowo prostuje. W efekcie sąsiednie cząsteczki które wcześniej, będąc małymi kulkami, najwyżej odbijały się od siebie, teraz zaczynają się przeplatać. Cysteiny z ich łańcuchów próbują utworzyć ponownie wiązania, aby powrócić do dawnego kształtu. Ponieważ jednak kłębek białka rozwinął się i splótł z sąsiednimi, nowo powstające mostki dwusiarczkowe łączą różne cząsteczki. W miejsce roztworu w pojedynczymi cząsteczkami powstaje trwała sieć.
Proces ten zużywa dość dużo energii. Co ciekawsze, mimo że temperatura ścinania żółtka jaja jest nieco niższa niż białka, to białko ścina się pierwsze. Wynika to z kiepskiego transportu ciepła oraz wspomnianego pochłaniania energii, zanim żółtko nagrzeje się na tyle, aby się ściąć, białko już dawno się dostatecznie nagrzało.
Naturacja?
Skoro sieć powstaje po utworzeniu przypadkowych połączeń między cząsteczkami białek, powinno być możliwe ich zerwanie oraz oddzielenie od siebie, aby nie kontaktujące się łańcuchy zwinęły się do rozpuszczalnej formy pierwotnej. Taki pomysł testował zespół badaczy pod kierunkiem profesora Gregory'ego Weissa [1]. Pomysł wziął się z prób izolowania pewnych białek powstających podczas procesów nowotworowych - mimo zastosowania ostrożnych warunków często białka izolowane z preparatów biologicznych wytrącały się w formie kłaczków oblepiających ścianki próbówek, będących masą splątanych łańcuchów.
Ale pewnego razu na konferencji zobaczył urządzenie, pozwalające dosłownie odrywać cząsteczki od siebie. Urządzenie (Vortex Fluid Device) wprowadza porcję płynu do tuby która wiruje z dużą prędkością co rozprowadza na jej powierzchni szybko poruszającą się, cienką warstwę. W warstwie tej ciecz porusza się niemal laminarnie, a na cząsteczki między jej warstwami działają duże siły ścinające. Proces ten pozwalał na przykład na oddzielenie od siebie warstw grafenu z cząstek grafitu.
Weiss sprowadził do siebie jedno takie urządzenie i przeprowadził eksperyment. Ugotował jajko na twardo i wyjął białą część. Rozdrobnione białko zmieszał z roztworem mocznika, związku który potrafi zrywać mostki siarczkowe między łańcuchami. W ten sposób wcześniej radzono sobie z denaturacją. Jednak nawet po rozbiciu sieci, wiele łańcuchów białka było ze sobą splątanych, gdy będąc wciąż blisko próbowały się zwinąć w kulkę. Zwykle z takiego roztworu dawało się odzyskać niewiele aktywnych białek.
Teraz jednak Weiss wprowadził roztwór rozpuszczonej w moczniku jajecznicy do urządzenia, którym siły ścinające działające na warstwę cieczy na powierzchni wirującej 5000 razy na minutę próbówki, odrywały poszczególne łańcuchy, tworząc roztwór odplątanych, odseparowanych protein. Po pięciu minutach wirowania, roztwór rozcieńczono buforem sprzyjającym powstawaniu formy natywnej. Dalsze badania wykazały, że udało się odzyskać 85% aktywnego lizozymu, ważnego białka przeciwbakteryjnego jaj kurzych.
Po co rozpuszczać ścięte białko? Niektóre białka są używane w biologii i medycynie, dla innych ich aktywność katalityczna pozwala je wykryć, co wykorzystują testy biomedyczne (przykładowo często oznaczany we krwi wskaźnik ALAT to poziom białkowego enzymu aminotransferazy alaninowej). Umiejętność przywracania im aktywnej formy po tym, jak wskutek niekorzystnych warunków podczas izolacji ścięły się jak się wydawało nieodwracalnie, może być więc bardzo przydatna.
Fizykochemia bezy
Proces denaturacji białka ma znaczenie też dla innego dania - piany białkowej a zwłaszcza jej słodkiej wersji czyli bez. Podczas roztrzepywania masy czysto fizyczne działanie trzepaczki powoduje, że część cząsteczek albuminy ulega rozwinięciu. Ponieważ ich wnętrza są hydrofobowe, rozwinięte cząsteczki przyklejają się do małych pęcherzyków powietrza, co tworzy stabilną pianę.
Denaturacja w tym przypadku jest jednak w dużym stopniu odwracalna - piana pozostawiona sama sobie po pewnym czasie wypuszcza bąbelki i rozpływa się, chyba że utrwalimy ją termicznie podczas wypieku.
Dawni kucharze dążący do tego, aby piana będąca podstawą lekkich kremów trzymała się długo i była sztywna, już dawno zauważyli że dobrą pianę otrzymuje się w naczyniach miedzianych lub srebrnych. Współcześnie wiemy, że ma to uzasadnienie - przenikające do ubijanej masy jony miedzi kompleksowały owomucynę, która przeszkadza w tworzeniu mostków dwusiarczkowych w surowym jaju, tym samym zwiększały trwałość piany [2]. Przy czym ilości te były śladowe i nie wpływały na smak.
Przy okazji przypominam mój stary wpis o naturalnych barwnikach do farbowania pisanek:
https://nowaalchemia.blogspot.com/2012/04/kraszanki-czyli-o-wielkanocnej-chemii.html
-------
[1] Gregory A. Weiss et al. Shear-Stress-Mediated Refolding of Proteins from Aggregates and Inclusion Bodies, Chem. bio. chem. Volume 16, Issue 3, Pages 393–396
[2] http://www.nature.com/nature/journal/v308/n5960/abs/308667a0.html
* https://www.washingtonpost.com/news/speaking-of-science/wp/2015/01/28/how-and-why-chemists-figured-out-how-to-unboil-an-egg/
* https://en.wikipedia.org/wiki/Egg_white
* https://en.wikipedia.org/wiki/Yolk
* https://en.wikipedia.org/wiki/Egg
* https://en.wikipedia.org/wiki/Denaturation_(biochemistry)
Jajo to jedna z faz rozwoju ptaków i gadów, w której niedojrzały zarodek zostaje wydalony poza organizm matki w otoczce odżywczego białka i tłuszczu zabezpieczonych twardą, nieprzenikalną skorupką. Jest także jednym z podstawowych produktów spożywczych.
Centralnie położone żółtko, będące głównym materiałem zapasowym rosnącego zarodka, zawiera więcej białek niż wodnisty płyn wokół nazywany białkiem. Jego żółty kolor to zasługa karotenoidów z karmy zjadanej przez kurę, głownie luteiny i zeaksantyny, dlatego odcień może różnić się zależnie od fermy i sposobu chowu, niekiedy gdy w karmie zawarta jest papryka, żółtko może wydawać się wręcz czerwone. Zawiera też tłuszcz zasobny w nienasycone kwasy tłuszczowe i znaczną ilość lecytyny będącej emulgatorem.
Pośrodku jaja utrzymują je elastyczne pasy chelazy.
Większość objętości jaja wypełnia wodniste białko zawierające, jak nazwa wskazuje, dużą ilość białek. Są to głównie albuminy, owotransferryna która kompleksuje żelazo, hamując wzrost bakterii, lizozym który niszczy bakterie Gram dodatnie, czy zapobiegająca przedwczesnemu ścinaniu owomucyna, będąca też głównym alergenem jaj.
Całość utrzymywana w szczelnej białkowej błonce, na którą organizm kury osadził twardą skorupkę zawierającą głównie węglan wapnia. Jej kolor zależy tylko od odmiany kury, w dużym stopniu też od upierzenia - lubiane na Zachodzie białe jajka znoszą głównie odmiany kur biało upierzonych, bardziej popularne u nas jasnobrązowe jaja składają głównie odmiany kur nakrapianych i brązowych, niektóre rasy dają jaja oliwkowe, nawet zielonkawe, albo ciemnobrązowe, z dodatkowymi kropkami.
Denaturacja
Proces ścinania, to jest zamiany formy białek z rozpuszczalnej w stałą, nazywany denaturacją. Może następować pod wpływem czynników fizycznych, a więc zmian temperatury, mechanicznego wytrząsania, naświetlania itp. ale też chemicznych jak jony metali ciężkich, mocne kwasy czy nawet wysokie stężenie soli.
W trakcie tego procesu następuje zmiana ukształtowania nici białkowej. Zwykle przybiera ona w naturze pewien określony kształt wymuszany przez oddziaływania aminokwasów, wiązania wodorowe czy mostki siarczkowe. Utrata tego pierwotnego kształtu zmienia właściwości białka, które może przestać pełnić swoją funkcję, na przykład enzymy stają się nieczynne katalitycznie. Jeśli zmiany te są odwracalne, a po użyciu korzystnych warunków (np. rozcieńczenie stężonego roztworu soli) białko wraca do poprzedniej formy, mówimy o denaturyzacji odwracalnej. Ale często dochodzi też do denaturyzacji nieodwracalnej, po której białko nawet w sprzyjających warunkach nie powróci do poprzedniej formy i funkcji. Enzymy usmażonego mięsa nie będą działać, a gumowata masa jajecznicy nie rozpłynie się po ochłodzeniu czy wymoczeniu w wodzie.
W kurzym jajku głównymi białkami wodnistej części są albuminy, zaliczane do globin, których cząsteczki mają kształt z grubsza kulisty, z hydrofobowymi częściami w środku. Z tego zresztą powodu rozpuszczają się w wodzie tworząc koloidy. Przy bliższym spojrzeniu ich cząsteczki wyglądają podobnie do luźnego kłębka wełny, którym niedawno bawił się kot.
Co jednak ważniejsze, w ich składzie dość często pojawia się siarka. Najczęściej jest to aminokwas cysteina. Jest to ważne, bowiem między dwoma atomami siarki w tej samej cząsteczce lubią się tworzyć mostki dwusiarczkowe, to jest wiązania -S-S-. Ich zaistnienie zmusza łańcuch aminokwasowy do zagięcia a więc w dużym stopniu decyduje o kształcie cząsteczki. Albuminy mogą zawierać kilka takich mostków, tworzących dość stabilną strukturę.
Sieciowanie
Co takiego następuje podczas gotowania? Duże drgania termiczne mają na tyle dużą energię, że mostki dwusiarczkowe ulegają zrywaniu, pękają wiązania wodorowe, zaś nić rozplątuje się i częściowo prostuje. W efekcie sąsiednie cząsteczki które wcześniej, będąc małymi kulkami, najwyżej odbijały się od siebie, teraz zaczynają się przeplatać. Cysteiny z ich łańcuchów próbują utworzyć ponownie wiązania, aby powrócić do dawnego kształtu. Ponieważ jednak kłębek białka rozwinął się i splótł z sąsiednimi, nowo powstające mostki dwusiarczkowe łączą różne cząsteczki. W miejsce roztworu w pojedynczymi cząsteczkami powstaje trwała sieć.
Proces ten zużywa dość dużo energii. Co ciekawsze, mimo że temperatura ścinania żółtka jaja jest nieco niższa niż białka, to białko ścina się pierwsze. Wynika to z kiepskiego transportu ciepła oraz wspomnianego pochłaniania energii, zanim żółtko nagrzeje się na tyle, aby się ściąć, białko już dawno się dostatecznie nagrzało.
Naturacja?
Skoro sieć powstaje po utworzeniu przypadkowych połączeń między cząsteczkami białek, powinno być możliwe ich zerwanie oraz oddzielenie od siebie, aby nie kontaktujące się łańcuchy zwinęły się do rozpuszczalnej formy pierwotnej. Taki pomysł testował zespół badaczy pod kierunkiem profesora Gregory'ego Weissa [1]. Pomysł wziął się z prób izolowania pewnych białek powstających podczas procesów nowotworowych - mimo zastosowania ostrożnych warunków często białka izolowane z preparatów biologicznych wytrącały się w formie kłaczków oblepiających ścianki próbówek, będących masą splątanych łańcuchów.
Ale pewnego razu na konferencji zobaczył urządzenie, pozwalające dosłownie odrywać cząsteczki od siebie. Urządzenie (Vortex Fluid Device) wprowadza porcję płynu do tuby która wiruje z dużą prędkością co rozprowadza na jej powierzchni szybko poruszającą się, cienką warstwę. W warstwie tej ciecz porusza się niemal laminarnie, a na cząsteczki między jej warstwami działają duże siły ścinające. Proces ten pozwalał na przykład na oddzielenie od siebie warstw grafenu z cząstek grafitu.
Weiss sprowadził do siebie jedno takie urządzenie i przeprowadził eksperyment. Ugotował jajko na twardo i wyjął białą część. Rozdrobnione białko zmieszał z roztworem mocznika, związku który potrafi zrywać mostki siarczkowe między łańcuchami. W ten sposób wcześniej radzono sobie z denaturacją. Jednak nawet po rozbiciu sieci, wiele łańcuchów białka było ze sobą splątanych, gdy będąc wciąż blisko próbowały się zwinąć w kulkę. Zwykle z takiego roztworu dawało się odzyskać niewiele aktywnych białek.
Teraz jednak Weiss wprowadził roztwór rozpuszczonej w moczniku jajecznicy do urządzenia, którym siły ścinające działające na warstwę cieczy na powierzchni wirującej 5000 razy na minutę próbówki, odrywały poszczególne łańcuchy, tworząc roztwór odplątanych, odseparowanych protein. Po pięciu minutach wirowania, roztwór rozcieńczono buforem sprzyjającym powstawaniu formy natywnej. Dalsze badania wykazały, że udało się odzyskać 85% aktywnego lizozymu, ważnego białka przeciwbakteryjnego jaj kurzych.
Po co rozpuszczać ścięte białko? Niektóre białka są używane w biologii i medycynie, dla innych ich aktywność katalityczna pozwala je wykryć, co wykorzystują testy biomedyczne (przykładowo często oznaczany we krwi wskaźnik ALAT to poziom białkowego enzymu aminotransferazy alaninowej). Umiejętność przywracania im aktywnej formy po tym, jak wskutek niekorzystnych warunków podczas izolacji ścięły się jak się wydawało nieodwracalnie, może być więc bardzo przydatna.
Fizykochemia bezy
Proces denaturacji białka ma znaczenie też dla innego dania - piany białkowej a zwłaszcza jej słodkiej wersji czyli bez. Podczas roztrzepywania masy czysto fizyczne działanie trzepaczki powoduje, że część cząsteczek albuminy ulega rozwinięciu. Ponieważ ich wnętrza są hydrofobowe, rozwinięte cząsteczki przyklejają się do małych pęcherzyków powietrza, co tworzy stabilną pianę.
Denaturacja w tym przypadku jest jednak w dużym stopniu odwracalna - piana pozostawiona sama sobie po pewnym czasie wypuszcza bąbelki i rozpływa się, chyba że utrwalimy ją termicznie podczas wypieku.
Dawni kucharze dążący do tego, aby piana będąca podstawą lekkich kremów trzymała się długo i była sztywna, już dawno zauważyli że dobrą pianę otrzymuje się w naczyniach miedzianych lub srebrnych. Współcześnie wiemy, że ma to uzasadnienie - przenikające do ubijanej masy jony miedzi kompleksowały owomucynę, która przeszkadza w tworzeniu mostków dwusiarczkowych w surowym jaju, tym samym zwiększały trwałość piany [2]. Przy czym ilości te były śladowe i nie wpływały na smak.
Przy okazji przypominam mój stary wpis o naturalnych barwnikach do farbowania pisanek:
https://nowaalchemia.blogspot.com/2012/04/kraszanki-czyli-o-wielkanocnej-chemii.html
-------
[1] Gregory A. Weiss et al. Shear-Stress-Mediated Refolding of Proteins from Aggregates and Inclusion Bodies, Chem. bio. chem. Volume 16, Issue 3, Pages 393–396
[2] http://www.nature.com/nature/journal/v308/n5960/abs/308667a0.html
* https://www.washingtonpost.com/news/speaking-of-science/wp/2015/01/28/how-and-why-chemists-figured-out-how-to-unboil-an-egg/
* https://en.wikipedia.org/wiki/Egg_white
* https://en.wikipedia.org/wiki/Yolk
* https://en.wikipedia.org/wiki/Egg
* https://en.wikipedia.org/wiki/Denaturation_(biochemistry)
piątek, 7 kwietnia 2017
Chemiczne rekordy (1.)
Czyli krótki opis substancji, które w czymś są wyjątkowe. Na razie rekordy bardziej fizyko-chemiczne.
Największa rozpuszczalność w wodzie i najgęstszy roztwór wodny
Rozpuszczalność jest miarą określającą jaka masa danego związku jest w stanie rozpuścić się w rozpuszczalniku. Silnie zależy od temperatury, zwykle jest podawana w gramach substancji na 100 gramów rozpuszczalnika. To jak duża będzie jej wartość oprócz zupełnie oczywistej kwestii siły oddziaływań między cząsteczkami, zależy też od masy molowej związku. Im większa będzie masa molowa, tym cięższa będzie ta sama ilość cząsteczek związku. Dla lekkiej wody jeden mol to 18 gramów, co przy gęstości około 1 g/cm3 daje nam mniej niż kieliszek. Dla azotanu potasu taka sama ilość cząsteczek waży 101 gramów. W 100 g wody rozpuścić się może ponad 300 g tego związku, czyli całe trzy mole.
Aby uzyskać wysoką rozpuszczalność w gramach na 100 g wody, należy więc znaleźć sól o stosunkowo wysokiej masie molowej, która dobrze się rozpuszcza. Palmę pierwszeństwa dzierży wśród prostych soli octan cezu. Wprawdzie molowa rozpuszczalność nie jest duża, bo wynosi około 5 mol/dm3 ale dzięki dużej masie molowej cezu, rozpuszczalność wynosi 1010 g/100g wody.
Oznacza to, że w szklance wody, rozpuścić mogą się ponad dwa kilogramy tej soli!
W mineralogii jedną z prostych metod rozpoznawania minerałów jest badanie gęstości względnej wobec gęstych cieczy - minerały mniej gęste pływają a gęstsze toną. Używa się w tym celu odpowiednio gęstych fluorowcowodorów, ale także roztworów wodnych o wysokiej gęstości, w tym nasyconego octanu cezu.
Nieco mniej rozpuszczalny od octanu mrówczan cezu, używany jest też jako płyn w płuczkach do głębokich odwiertów, na przykład ropy naftowej, aby utrzymywać w nich nacisk zapobiegający nagłym wyrzutom gazów. Nasycony roztwór ma gęstość 2,3 g/cm3.
Jeszcze większą gęstość, mimo mniejszej rozpuszczalności, można uzyskać dla nasyconego roztworu wolframianu cezu WO4Cs2, wynosi ona 2,9 g/cm3 co oznacza, że pływa w nim beton. Następny w kolejności jest poliwolframian sodu którego roztwór osiąga 3,1 g/cm3. Ale rekordzistą pod tym względem jest tzw. roztwór Clerici.
Jest to roztwór mieszaniny mrówczanu i malonianu talu, innego ciężkiego pierwiastka o własnościach podobnych do metali alkalicznych. Przy odpowiednio dobranej proporcji roztwór ma w temperaturze pokojowej gęstość 4,25 g/cm3, co oznacza że pływa w nim diament a tonie cyrkonia.
W praktyce jest rzadko używany ze względu na korozyjność i fakt, że rozpuszczalne sole talu są silnie trujące.
Najcięższy gaz
Najlżejszym gazem w warunkach standardowych jest wodór, znany z baloników hel jest od niego nieco bardziej gęsty. A jaki gaz jest najcięższy?
Gazem o największej gęstości w warunkach standardowych, jest sześciofluorek wolframu. Jego gęstość to 13 g/l jest więc około 11 razy cięższy od powietrza. To gaz bezbarwny, trujący, hydrolizujący w wodzie z wydzieleniem fluorowodoru, powodujący obrzęk płuc. Poniżej temperatury 17*C skrapla się do żółtawej cieczy.
W przemyśle jest używany do osadzania warstewki wolframu na ogrzanych powierzchniach, jego wytwarzanie i destylacja są też sposobem na otrzymanie metalu wysokiej czystości.
Innym bardzo gęstym gazem jest czysty radon, nietrwały pierwiastek promieniotwórczy z grupy gazów szlachetnych. Jego gęstość to 9 g/l.
Najbardziej znanym gęstym gazem, który wdychany powoduje niesamowite pogrubienie głosu, jest sześciofluorek siarki, obojętny i nietoksyczny gaz o gęstości 6 g/l. Możliwe jest na przykład umieszczenie łódki z folii tak, aby pływała na zebranej w naczyniu warstwie.
Najgęstsza ciecz
Najgęstszą cieczą (w warunkach standardowych) jest metaliczna rtęć o gęstości 13,5 g/cm3. Jak na metal tworzy bardzo słabe wiązania metaliczne stąd bardzo niska temperatura topnienia -38,8*C. Zastanawiałem się czy nieco gęstsze nie będą niektóre ciekłe amalgamaty, ale wygląda na to, że dodatek jakiegokolwiek metalu zmniejsza gęstość powstałego połączenia.
-------
* https://en.wikipedia.org/wiki/Clerici_solution
* https://en.wikipedia.org/wiki/Density
Największa rozpuszczalność w wodzie i najgęstszy roztwór wodny
Rozpuszczalność jest miarą określającą jaka masa danego związku jest w stanie rozpuścić się w rozpuszczalniku. Silnie zależy od temperatury, zwykle jest podawana w gramach substancji na 100 gramów rozpuszczalnika. To jak duża będzie jej wartość oprócz zupełnie oczywistej kwestii siły oddziaływań między cząsteczkami, zależy też od masy molowej związku. Im większa będzie masa molowa, tym cięższa będzie ta sama ilość cząsteczek związku. Dla lekkiej wody jeden mol to 18 gramów, co przy gęstości około 1 g/cm3 daje nam mniej niż kieliszek. Dla azotanu potasu taka sama ilość cząsteczek waży 101 gramów. W 100 g wody rozpuścić się może ponad 300 g tego związku, czyli całe trzy mole.
Aby uzyskać wysoką rozpuszczalność w gramach na 100 g wody, należy więc znaleźć sól o stosunkowo wysokiej masie molowej, która dobrze się rozpuszcza. Palmę pierwszeństwa dzierży wśród prostych soli octan cezu. Wprawdzie molowa rozpuszczalność nie jest duża, bo wynosi około 5 mol/dm3 ale dzięki dużej masie molowej cezu, rozpuszczalność wynosi 1010 g/100g wody.
Oznacza to, że w szklance wody, rozpuścić mogą się ponad dwa kilogramy tej soli!
W mineralogii jedną z prostych metod rozpoznawania minerałów jest badanie gęstości względnej wobec gęstych cieczy - minerały mniej gęste pływają a gęstsze toną. Używa się w tym celu odpowiednio gęstych fluorowcowodorów, ale także roztworów wodnych o wysokiej gęstości, w tym nasyconego octanu cezu.
Nieco mniej rozpuszczalny od octanu mrówczan cezu, używany jest też jako płyn w płuczkach do głębokich odwiertów, na przykład ropy naftowej, aby utrzymywać w nich nacisk zapobiegający nagłym wyrzutom gazów. Nasycony roztwór ma gęstość 2,3 g/cm3.
Jeszcze większą gęstość, mimo mniejszej rozpuszczalności, można uzyskać dla nasyconego roztworu wolframianu cezu WO4Cs2, wynosi ona 2,9 g/cm3 co oznacza, że pływa w nim beton. Następny w kolejności jest poliwolframian sodu którego roztwór osiąga 3,1 g/cm3. Ale rekordzistą pod tym względem jest tzw. roztwór Clerici.
Jest to roztwór mieszaniny mrówczanu i malonianu talu, innego ciężkiego pierwiastka o własnościach podobnych do metali alkalicznych. Przy odpowiednio dobranej proporcji roztwór ma w temperaturze pokojowej gęstość 4,25 g/cm3, co oznacza że pływa w nim diament a tonie cyrkonia.
W praktyce jest rzadko używany ze względu na korozyjność i fakt, że rozpuszczalne sole talu są silnie trujące.
Najcięższy gaz
Najlżejszym gazem w warunkach standardowych jest wodór, znany z baloników hel jest od niego nieco bardziej gęsty. A jaki gaz jest najcięższy?
Gazem o największej gęstości w warunkach standardowych, jest sześciofluorek wolframu. Jego gęstość to 13 g/l jest więc około 11 razy cięższy od powietrza. To gaz bezbarwny, trujący, hydrolizujący w wodzie z wydzieleniem fluorowodoru, powodujący obrzęk płuc. Poniżej temperatury 17*C skrapla się do żółtawej cieczy.
W przemyśle jest używany do osadzania warstewki wolframu na ogrzanych powierzchniach, jego wytwarzanie i destylacja są też sposobem na otrzymanie metalu wysokiej czystości.
Innym bardzo gęstym gazem jest czysty radon, nietrwały pierwiastek promieniotwórczy z grupy gazów szlachetnych. Jego gęstość to 9 g/l.
Najbardziej znanym gęstym gazem, który wdychany powoduje niesamowite pogrubienie głosu, jest sześciofluorek siarki, obojętny i nietoksyczny gaz o gęstości 6 g/l. Możliwe jest na przykład umieszczenie łódki z folii tak, aby pływała na zebranej w naczyniu warstwie.
Najgęstsza ciecz
Najgęstszą cieczą (w warunkach standardowych) jest metaliczna rtęć o gęstości 13,5 g/cm3. Jak na metal tworzy bardzo słabe wiązania metaliczne stąd bardzo niska temperatura topnienia -38,8*C. Zastanawiałem się czy nieco gęstsze nie będą niektóre ciekłe amalgamaty, ale wygląda na to, że dodatek jakiegokolwiek metalu zmniejsza gęstość powstałego połączenia.
-------
* https://en.wikipedia.org/wiki/Clerici_solution
* https://en.wikipedia.org/wiki/Density
poniedziałek, 3 kwietnia 2017
To już szósty rok!
To nie żart, minął szósty rok na tym blogu.
Zacznę od podsumowania wewnętrznych statystyk:
Blog wyświetlano 890 tysięcy razy, toteż od zeszłego roku przybyło 200 tysięcy, szacuję że niestety jakieś 10-15% to wejścia botów
- średnia dzienna przeglądalność to około 500-600 wyświetleń
- przybyło 120 komentarzy
Kilka artykułów opublikowanych w ciągu tego roku wywołało większe zainteresowanie, szczególnie "Witamina lewa i prawa" który przeczytano 24 tysiące razy, co dało mu ostatecznie drugie miejsce wśród najpopularniejszych (wpis o Ałunie jest nie do pobicia). Chętnie czytano też artykuł "Co to jest ksylitol?" wyświetlony 12 tysięcy razy, oraz "Dlaczego osm jest najgęstszym pierwiastkiem?" wyświetlony 11 tysięcy razy - co było dla mnie pewnym zaskoczeniem, bo niekoniecznie jest to łatwa tematyka.
Do sukcesów minionego roku mogę też zaliczyć nawiązanie współpracy z "Przekrojem" w czym fakt istnienia tego bloga miał pewien udział.
Jeśli chodzi o plany, mam nadzieję że uda się wystartować z serią wpisów z propozycjami małych doświadczeń do wykonania w domu, kuchni, garażu czy ostatecznie na szkolnej pracowni chemicznej. Na razie robię parapetowe próby z czym uda się najprościej, bez specjalistycznych zakupów
Zacznę od podsumowania wewnętrznych statystyk:
Blog wyświetlano 890 tysięcy razy, toteż od zeszłego roku przybyło 200 tysięcy, szacuję że niestety jakieś 10-15% to wejścia botów
- średnia dzienna przeglądalność to około 500-600 wyświetleń
- przybyło 120 komentarzy
Kilka artykułów opublikowanych w ciągu tego roku wywołało większe zainteresowanie, szczególnie "Witamina lewa i prawa" który przeczytano 24 tysiące razy, co dało mu ostatecznie drugie miejsce wśród najpopularniejszych (wpis o Ałunie jest nie do pobicia). Chętnie czytano też artykuł "Co to jest ksylitol?" wyświetlony 12 tysięcy razy, oraz "Dlaczego osm jest najgęstszym pierwiastkiem?" wyświetlony 11 tysięcy razy - co było dla mnie pewnym zaskoczeniem, bo niekoniecznie jest to łatwa tematyka.
Jeśli chodzi o plany, mam nadzieję że uda się wystartować z serią wpisów z propozycjami małych doświadczeń do wykonania w domu, kuchni, garażu czy ostatecznie na szkolnej pracowni chemicznej. Na razie robię parapetowe próby z czym uda się najprościej, bez specjalistycznych zakupów
środa, 29 marca 2017
Żywność z mikrofalówki
W ciągu ostatnich kilkunastu lat kuchenki mikrofalowe stały się takim powszechnym sprzętem domowym, jak zmywarki czy roboty kuchenne. Ze względu na swój nieoczywisty sposób działania obrosły jednak wieloma mitami. W tym też takimi, jakie mogą zainteresować chemika.
Jak działa mikrofalówka?
Mikrofale są falami promieniowania elektromagnetycznego, podobnie jak fale radiowe czy światło widzialne. Oznacza to, że w punkcie przestrzeni przez który przechodzą, pojawia się pole elektryczne i magnetyczne, których wektor natężenia (kierunek w którym następuje zmiana) zmienia zwrot co pewien okres, zależny od częstotliwości.
Dość arbitralnie uznaje się za mikrofale, falę o długości (odległość w przestrzeni między dwoma punktami o takim samym wektorze pola) od 1 mm do 30 cm. Niosą więcej energii niż dłuższe fale radiowe, ale mniej niż krótsza podczerwień.
Ogrzewanie przez nie ciał następuje wskutek oddziaływania z dipolami. Jeśli cząsteczka związku chemicznego ma nierównomiernie i niesymetrycznie rozłożony ładunek elektryczny, to nabiera momentu dipolowego, to jest zachowuje się jak układ leżących blisko ładunku dodatniego i ujemnego. Następuje to wtedy, gdy tworzą ją atomy różniące się elektroujemnością, to jest zdolnością do przyciągania elektronów, i nie są ułożone tak, że posiadają środek symetrii. W przeciwnym przypadku części cząsteczki powtarzające się po obu stronach tegoż środka ściągałyby ładunek w przeciwne strony i nie było by żadnego wyróżnionego kierunku.
Zerowy moment dipolowy ma liniowa cząsteczka dwutlenku węgla, a wyraźny niezerowy na przykład cząsteczka wody.
Dipole, które zachowują się jak układ przeciwnych ładunków, reagują na pola elektryczne lub magnetyczne. W stałym, dostatecznie silnym polu, będą się obracać równolegle do wektora jego siły, tak aby do źródła mającego ładunek dodatni lub ujemny obrócony był fragment cząsteczki o przeciwnym ładunku.
Podobnie rzecz się ma gdy na dipol oddziałuje fala elektromagnetyczna - cząsteczka wpada w zmienne pole, którego wektor co chwila zmienia się, wskazując raz to w jedną raz to w przeciwną stronę. W przypadku fal krótkich, jak dla światła widzialnego, gdzie długość fali jest liczona w nanometrach, czas przez jaki cząsteczka omiatana falą znajduje się w polu o jednym kierunku jest tak krótki, że nie nadąża zareagować. W przypadku długich, jak fale radiowe, wprawdzie pozostaje ona w polu danego kierunku długo, ale sama fala niesie ze sobą niską energię. Pośrodku znalazły się mikrofale - na tyle długie, aby cząsteczka zdążała zareagować, i zarazem niosące dostatecznie dużo energii aby po jej otrzymaniu cząsteczka pokonała swoją bezwładność.
W skrócie - cząsteczki będące dipolami w polu elektrycznym będącym składową mikrofal, zaczynają drgać. A drgania całych cząsteczek to właśnie to, co fizycy nazywają temperaturą. Energia kinetyczna rozedrganych mikrofalami cząsteczek dipola rozchodzi się przez oddziaływanie z innymi cząsteczkami. Mikrofalówki domowe posiadają źródła mikrofal o częstotliwości 2,45 GHz, co odpowiada długości fali 12,2 cm. Fala tej długości działa przede wszystkim na cząsteczki wody, posiadające wyraźny moment dipolowy. To od wody rozgrzewa się całe danie. Fale wnikają wgłąb porcji na 2-3 cm, co w zasadzie oznacza, że przenikają ją całą od momentu włączenia.
Ten typ ogrzewania różni się od konwencjonalnego przede wszystkim szybkością - w przypadku gotowanej kiełbaski rozchodzenie się ciepła następuje od zewnątrz do środka. Najpierw zużywamy ciepło na zagotowanie wody. Potem woda przekazuje energię zewnętrznym warstwom kiełbaski, te poprzez oddziaływania cząsteczek przekazują energię warstwom głębszym i tak dalej aż całość ogrzeje się na tyle, aby dało się to zjeść. Bywa że większe kawały mięsa zostają niedogotowane w środku. To rozchodzenie się ciepła nie jest zbyt szybkie, praktycznie żadnej roli nie pełni tu konwekcja wody wewnątrz jedzenia, mięso czy tkanki roślinne zwykle nie są zbyt dobrymi przewodnikami ciepła. Trzeba więc utrzymywać w stanie wrzenia wodę z naszą kiełbaską odpowiednio długo.
Mikrofale przenikają porcję jedzenia od razu od momentu włączenia, a ciepło jest wytwarzane w środku, przez co uzyskanie tej samej temperatury następuje krócej. Jedzenie jest wręcz cieplejsze w środku niż na zewnątrz, ze względu na wypromieniowanie ciepła przez powierzchnię, mającą kontakt z wcale nie gorącym powietrzem. Ma to pewien paradoksalny skutek, możliwy do zaobserwowania w doświadczeniu z kostkami sera - na talerz mikrofalówki kładziemy kostki żółtego sera, jedną dużą drugą mniejszą. Po włączeniu na średnią moc możemy zauważyć, że większa kostka stopi się szybciej.
Fale używane w kuchence mikrofalowej mają długość 12,2 cm. Są zatrzymywane przez metalową siatkę widoczną w szkle drzwiczek, ale obecną też w ściankach, której oczka są dużo mniejsze.
Utrata witamin
Teksty temat tego jak bardzo złe jest ogrzewanie jedzenia w mikrofalówce najczęściej powtarzają twierdzenie, że mikrofala "wyjaławia żywność" lub "niszczy wszystkie składniki odżywcze". W tym wyjaławianiu coś jest na rzeczy, bo podgrzanie jedzenia zwykle zabija bakterie, a w tym przypadku równomierne rozgrzanie od środka rozwiązuje problem niedosmażenia mięsiwa. Jak jednak wygląda sprawa składników odżywczych? W końcu takie na przykład witaminy są często wrażliwe na obróbkę cieplną.
Podczas ogrzewania część witamin bądź rozkłada się, bądź utlenia. Na to jak dużo substancji przereaguje, oprócz temperatury wpływ ma też czas trwania procesu. Jeśli w mikrofali osiągnięcie tego samego podgrzania następuje szybciej, można spodziewać się mniejszych strat witamin. I to pokazały badania. Znalazłem obszerny polskojęzyczny przegląd prac na ten temat.
Dla witaminy C stwierdzono, że ogrzewanie w mikrofali brokułów wywołuje mniejsze straty niż podczas zwykłego gotowania, porównywalnie małe dawało gotowanie pod ciśnieniem. Gotowanie tak ziemniaków, kalafiora, brukselki i fasolki szparagowej dawało straty znacząco mniejsze niż dla gotowania zwykłego. [1]
Dla witaminy B1 obserwowane straty przy gotowaniu mikrofalowym były bądź porównywalne (dla ciecierzycy) lub nieco mniejsze (dla boćwiny i zielonej fasolki) niż w zwykłym gotowaniu. Dla witaminy B2 straty w mikrofali były porównywalne lub mniejsze, z wyjątkiem zielonego groszku gdzie były większe. Dla witaminy PP straty w gotowanej ciecierzycy były mniejsze. [2]
Polifenole
Do najczęściej powtarzanych argumentów należy niszczenie polifenoli i flawonoidów podczas ogrzewania w mikrofali. Niekiedy artykuły powołują się na konkretne badanie, w którym stwierdzono, że w gotowanych tak brokułach zawartość tych związków spada aż o 97%. Faktycznie, takie dane pojawiają się w cytowanym badaniu. Artykuły jednak nie są chętne wejść w szczegóły - brokuły były w tym badaniu gotowane w wodzie przy pomocy mikrofal, większość strat polifenoli wynikała nie z rozkładu tylko z rozpuszczenia się ich w wodzie, którą wylewano. W czasie tego samego badania stwierdzono też stratę 66% polifenoli podczas gotowania tradycyjnego.[3]
Sami autorzy przyznają zresztą, że te wyniki znacząco odbiegają od uzyskanych w innych badaniach, przykładowo japońscy badacze badający gotowanie cebuli stwierdzili, że między gotowaniem tradycyjnym a mikrofalowym nie ma różnicy dla strat polifenoli [4] a indyjski zespól badający w ten sposób 14 warzyw stwierdził, że straty podczas gotowania na parze i w mikrofali były mniejsze niż podczas gotowania zwykłego.[5]
Tak, że no owszem, bardzo dużą stratę zawartości polifenoli stwierdzono, ale tylko w jednym badaniu. Ponieważ główną przyczyną strat było rozpuszczanie polifenoli w wodzie którą potem odlewano, można się domyśleć, że w przypadku potraw których część stanowią warzywa, i z których nie odlewa się wody, straty będą bardzo małe.
Zmiana kształtu białek
Kolejnym częstym argumentem, jest zmienianie kształtu białek i powodowanie, że stają się nienaturalne. A jeśli coś jest nienaturalne to organizm tego nie poznaje i nie trawi.
Jest to kolejna wieść z kategorii "coś dzwoni ale nie wiadomo w którym uniwersytecie". Owszem, ogrzewanie żywności w mikrofalówce zmienia struktury białek, i to na takie których w naturze nie ma. Tylko że nie jest to nic nadzwyczajnego, zachodzi też podczas smażenia i gotowania. Proces ten nazywa się denaturacją. Przykładowo podczas smażenia jajecznicy rozpuszczalne w wodzie albuminy, będące białkami o cząsteczkach w kształcie kłębków sznurka, rozwijają się i prostują, po czym tworzą siatkę wielu przeplecionych łańcuchów. Taka struktura nie występuje w naturze. Jednak organizm nie ma z nią żadnego problemu. Nasz żołądek nie trudni się rozpoznawaniem struktury białka i testowaniem naturalności konformacji, tylko wytwarza enzymy które tą strukturę naturalną czy nie, niszczą i trawią.
Izomeryzacja aminokwasów
W paru miejscach widziałem, że dla udowodnienia szkodliwego wpływu powoływano się na badania na temat izomeryzacji aminokwasów.[6] Jak to już było tłumaczone we wpisie o witaminie C, w pewnych przypadkach asymetria cząsteczki powoduje, że związki chemiczne mogą posiadać dwie formy, podobne jak lustrzane odbicia ale nie nakładające się.
Takimi związkami są na przykład alfa-aminokwasy budujące białka, ale też często występujące w organizmach swobodnie. Spośród dwóch podobnych form - L i D, w organizmach żywych występują praktycznie tylko aminokwasy L.
No i otóż, jak wykazano podczas ogrzewania mleka w mikrofali, część wolnych aminokwasów ulega izomeryzacji w nienaturalną formę D. Co to powoduje? Wedle artykułów szkodzi i ma uzasadniać szkodliwość mikrofalówek.
Czy D-aminokwasy, które normalnie nie wchodzą w skład białek żywych organizmów, nie występują w przyrodzie i pojawiają się dopiero po nienaturalnym ogrzaniu mikrofalami? Nie.
Nie są zbyt częste, ale pojawiają się w organizmach i żywności wskutek spontanicznej izomeryzacji. Reakcja taka, jak wiele innych, ma pewną określoną szybkość, która zwiększa się po ogrzaniu. I to zupełnie niezależnie od sposobu ogrzewania.
W pewnym badaniu ogrzewano mleko bądź w mikrofalówce lub konwencjonalnie i zbadano zawartość izomerów D kwasu asparaginowego i glutaminowego. Przed ogrzaniem mleko zawierało około 0,4-0,45% tych izomerów, po ogrzaniu zarówno mikrofalowym jak i zwykłym ich zawartość zwiększyła się o 0,25%. Między próbkami ogrzewanymi na różne sposoby przez ten sam czas nie było różnic w zawartości D-izomerów.[7]
W zasadzie z uwagi na to, że mikrofalami można ogrzać mleko szybciej, można by się spodziewać mniejszych poziomów tych izomerów.
Wspomniane izomery D nie są tak znów nienaturalne, skoro dokładne badania wykazują ich niewielkie ilości w różnych produktach naturalnych. W obszernym przeglądzie badań stwierdzono na przykład, że izomery aminokwasów białkowych występują zarówno w mleku surowym jak i pasteryzowanym. Większe ilości pojawiają się w produktach fermentowanych, a więc kefirze, jogurcie i serach, zwłaszcza w serze długo dojrzewającym, wskutek metabolizmu bakterii. Śladowe ilości pojawiają się w mięsie kurczaka i bekonie, i zwiększają po smażeniu, a nawet w chlebie gdzie podpieczenie tosta zwiększa poziom D-aminokwasów prawie dwa razy.[8]
Wykrywa się je także w ludzkim organizmie i podejrzewa, że mogą pełnić pewne funkcje biologiczne, być na przykład neuroprzekaźnikami, trudno więc straszyć ich obecnością.
Enzymy
W paru artykułach wspomniano o niszczeniu przez mikrofale enzymów z jedzenia. To prawda, ale przyczyną jest samo podgrzanie. Enzymy są białkami a wysoka temperatura zmienia ich strukturę i je unieczynnia. Nie ma znaczenia w jaki sposób odbywa się ogrzanie.
Nitrozoaminy
Nitrozoaminy to rakotwórcze produkty reakcji zachodzących w wysokiej temperaturze między aminami i azotynami. Pojawiają się w przetworzonym mięsie podczas pieczenia i smażenia. Artykuły o mikrofalówkach często twierdzą, że podczas ogrzewania w nich tworzy się konkretnie d-nitrozodietanoloamina (NDMA), trudno powiedzieć czemu akurat ta. Są badania na temat powstawania nitrozoamin w ogóle. Na przykład porównując boczek pieczony w mikrofali ze smażonym na patelni, stwierdzono powstawanie nitrozoamin w obu, w tym smażonym w większej ilości.[9]
W badaniu zawartości NDMA w koreańskich owocach morza ogrzewanych na sześć różnych sposobów, stwierdzono że najwyższe poziomy tej substancji powstawały podczas ogrzewania na grillu na węgiel drzewny, a najmniejsze przy ogrzaniu w mikrofalówce i gotowaniu w ciśnieniowej kuchence parowej.[10]
Inne dziwaczne argumenty
Artykuły o mikrofalówkach często są doprawione dziwacznymi wieściami, które w zasadzie nie stanowią żadnych argumentów, ale mają robić atmosferę. Do najczęściej powtarzanych należy wiadomość że ZSRR zakazało domowych mikrofalówek ze względu na dbanie o zdrowie obywateli, tylko nie wiadomo kiedy - daty wahają się od lat 50 do lat 80. Czasem pojawia się twierdzenie, że wynaleźli ją Naziści.
Inną często przytaczaną opowieścią jest śmierć pacjenta któremu przetoczono krew, wcześniej podgrzaną w mikrofalówce, oczywiście wskutek szkodliwego wpływu mikrofal na krew. Taka historia faktycznie miała miejsce w 1989 roku w stanie Oklahoma w USA. Ale przyczyna śmierci była inna - pielęgniarka miała ogrzać krew przechowywaną w lodówce do temperatury ciała pacjenta. Zamiast użyć standardowej łaźni z ciepłą wodą, użyła mikrofali, określając potrzebny czas na wyczucie. W efekcie krew zamiast ogrzać się do tych około 36 stopni, przegrzała się. Wprawdzie ochłodzono ją ale z powodu za wysokiej temperatury doszło do częściowej hemolizy, czyli pęknięcia czerwonych krwinek. Po wprowadzeniu jej do krążenia pojawiły się skrzepy, będąc przyczyną śmierci pacjentki. W 1995 roku rodzina zmarłej dostała odszkodowanie.[11]
Do tego dochodzą takie dziwne twierdzenia jak gromadzenie się mikrofal w jedzeniu, wodzie a nawet meblach kuchennych (!).
Prawdziwy problem
Prawdziwy problem w żywności z mikrofalówki jest taki, że niezbyt dobrą jakość ma żywność do niej wkładania. Gotowe zestawy do podgrzania to często już na wstępie mocno przetworzona żywność z dużą ilością tłuszczy, małą błonnika i witamin. Nie powinny stanowić podstawowej diety w ciągu dnia.
--------
[1] http://www.ptfarm.pl/pub/File/Bromatologia/2013/3/BR%203-2013%20s.%20241-249.pdf
[2] https://www.ptfarm.pl/pub/File/Bromatologia/2013/3/BR%203-2013%20s.%20250-257.pdf
[3] http://www.ingentaconnect.com/content/jws/jsfa/2003/00000083/00000014/art00018;jsessionid=1smkxaf0ymund.victoria
[4] https://www.ncbi.nlm.nih.gov/pubmed/11349895
[5] http://www.ijfans.com/vol2issue3/9.pdf
[6] https://www.ncbi.nlm.nih.gov/pubmed/1968186
[7] https://www.ncbi.nlm.nih.gov/pubmed/7911811
[8] http://www.acta.sapientia.ro/acta-alim/C2-1/alim2-1.pdf
[9] https://www.ncbi.nlm.nih.gov/pubmed/2307266
[10] http://www.tandfonline.com/doi/abs/10.1080/0265203021000014770
[11] http://wyomcases.courts.state.wy.us/applications/oscn/DeliverDocument.asp?citeID=4387
Jak działa mikrofalówka?
Mikrofale są falami promieniowania elektromagnetycznego, podobnie jak fale radiowe czy światło widzialne. Oznacza to, że w punkcie przestrzeni przez który przechodzą, pojawia się pole elektryczne i magnetyczne, których wektor natężenia (kierunek w którym następuje zmiana) zmienia zwrot co pewien okres, zależny od częstotliwości.
Dość arbitralnie uznaje się za mikrofale, falę o długości (odległość w przestrzeni między dwoma punktami o takim samym wektorze pola) od 1 mm do 30 cm. Niosą więcej energii niż dłuższe fale radiowe, ale mniej niż krótsza podczerwień.
Ogrzewanie przez nie ciał następuje wskutek oddziaływania z dipolami. Jeśli cząsteczka związku chemicznego ma nierównomiernie i niesymetrycznie rozłożony ładunek elektryczny, to nabiera momentu dipolowego, to jest zachowuje się jak układ leżących blisko ładunku dodatniego i ujemnego. Następuje to wtedy, gdy tworzą ją atomy różniące się elektroujemnością, to jest zdolnością do przyciągania elektronów, i nie są ułożone tak, że posiadają środek symetrii. W przeciwnym przypadku części cząsteczki powtarzające się po obu stronach tegoż środka ściągałyby ładunek w przeciwne strony i nie było by żadnego wyróżnionego kierunku.
Zerowy moment dipolowy ma liniowa cząsteczka dwutlenku węgla, a wyraźny niezerowy na przykład cząsteczka wody.
Dipole, które zachowują się jak układ przeciwnych ładunków, reagują na pola elektryczne lub magnetyczne. W stałym, dostatecznie silnym polu, będą się obracać równolegle do wektora jego siły, tak aby do źródła mającego ładunek dodatni lub ujemny obrócony był fragment cząsteczki o przeciwnym ładunku.
Podobnie rzecz się ma gdy na dipol oddziałuje fala elektromagnetyczna - cząsteczka wpada w zmienne pole, którego wektor co chwila zmienia się, wskazując raz to w jedną raz to w przeciwną stronę. W przypadku fal krótkich, jak dla światła widzialnego, gdzie długość fali jest liczona w nanometrach, czas przez jaki cząsteczka omiatana falą znajduje się w polu o jednym kierunku jest tak krótki, że nie nadąża zareagować. W przypadku długich, jak fale radiowe, wprawdzie pozostaje ona w polu danego kierunku długo, ale sama fala niesie ze sobą niską energię. Pośrodku znalazły się mikrofale - na tyle długie, aby cząsteczka zdążała zareagować, i zarazem niosące dostatecznie dużo energii aby po jej otrzymaniu cząsteczka pokonała swoją bezwładność.
W skrócie - cząsteczki będące dipolami w polu elektrycznym będącym składową mikrofal, zaczynają drgać. A drgania całych cząsteczek to właśnie to, co fizycy nazywają temperaturą. Energia kinetyczna rozedrganych mikrofalami cząsteczek dipola rozchodzi się przez oddziaływanie z innymi cząsteczkami. Mikrofalówki domowe posiadają źródła mikrofal o częstotliwości 2,45 GHz, co odpowiada długości fali 12,2 cm. Fala tej długości działa przede wszystkim na cząsteczki wody, posiadające wyraźny moment dipolowy. To od wody rozgrzewa się całe danie. Fale wnikają wgłąb porcji na 2-3 cm, co w zasadzie oznacza, że przenikają ją całą od momentu włączenia.
Ten typ ogrzewania różni się od konwencjonalnego przede wszystkim szybkością - w przypadku gotowanej kiełbaski rozchodzenie się ciepła następuje od zewnątrz do środka. Najpierw zużywamy ciepło na zagotowanie wody. Potem woda przekazuje energię zewnętrznym warstwom kiełbaski, te poprzez oddziaływania cząsteczek przekazują energię warstwom głębszym i tak dalej aż całość ogrzeje się na tyle, aby dało się to zjeść. Bywa że większe kawały mięsa zostają niedogotowane w środku. To rozchodzenie się ciepła nie jest zbyt szybkie, praktycznie żadnej roli nie pełni tu konwekcja wody wewnątrz jedzenia, mięso czy tkanki roślinne zwykle nie są zbyt dobrymi przewodnikami ciepła. Trzeba więc utrzymywać w stanie wrzenia wodę z naszą kiełbaską odpowiednio długo.
Mikrofale przenikają porcję jedzenia od razu od momentu włączenia, a ciepło jest wytwarzane w środku, przez co uzyskanie tej samej temperatury następuje krócej. Jedzenie jest wręcz cieplejsze w środku niż na zewnątrz, ze względu na wypromieniowanie ciepła przez powierzchnię, mającą kontakt z wcale nie gorącym powietrzem. Ma to pewien paradoksalny skutek, możliwy do zaobserwowania w doświadczeniu z kostkami sera - na talerz mikrofalówki kładziemy kostki żółtego sera, jedną dużą drugą mniejszą. Po włączeniu na średnią moc możemy zauważyć, że większa kostka stopi się szybciej.
Fale używane w kuchence mikrofalowej mają długość 12,2 cm. Są zatrzymywane przez metalową siatkę widoczną w szkle drzwiczek, ale obecną też w ściankach, której oczka są dużo mniejsze.
Utrata witamin
Teksty temat tego jak bardzo złe jest ogrzewanie jedzenia w mikrofalówce najczęściej powtarzają twierdzenie, że mikrofala "wyjaławia żywność" lub "niszczy wszystkie składniki odżywcze". W tym wyjaławianiu coś jest na rzeczy, bo podgrzanie jedzenia zwykle zabija bakterie, a w tym przypadku równomierne rozgrzanie od środka rozwiązuje problem niedosmażenia mięsiwa. Jak jednak wygląda sprawa składników odżywczych? W końcu takie na przykład witaminy są często wrażliwe na obróbkę cieplną.
Podczas ogrzewania część witamin bądź rozkłada się, bądź utlenia. Na to jak dużo substancji przereaguje, oprócz temperatury wpływ ma też czas trwania procesu. Jeśli w mikrofali osiągnięcie tego samego podgrzania następuje szybciej, można spodziewać się mniejszych strat witamin. I to pokazały badania. Znalazłem obszerny polskojęzyczny przegląd prac na ten temat.
Dla witaminy C stwierdzono, że ogrzewanie w mikrofali brokułów wywołuje mniejsze straty niż podczas zwykłego gotowania, porównywalnie małe dawało gotowanie pod ciśnieniem. Gotowanie tak ziemniaków, kalafiora, brukselki i fasolki szparagowej dawało straty znacząco mniejsze niż dla gotowania zwykłego. [1]
Dla witaminy B1 obserwowane straty przy gotowaniu mikrofalowym były bądź porównywalne (dla ciecierzycy) lub nieco mniejsze (dla boćwiny i zielonej fasolki) niż w zwykłym gotowaniu. Dla witaminy B2 straty w mikrofali były porównywalne lub mniejsze, z wyjątkiem zielonego groszku gdzie były większe. Dla witaminy PP straty w gotowanej ciecierzycy były mniejsze. [2]
Polifenole
Do najczęściej powtarzanych argumentów należy niszczenie polifenoli i flawonoidów podczas ogrzewania w mikrofali. Niekiedy artykuły powołują się na konkretne badanie, w którym stwierdzono, że w gotowanych tak brokułach zawartość tych związków spada aż o 97%. Faktycznie, takie dane pojawiają się w cytowanym badaniu. Artykuły jednak nie są chętne wejść w szczegóły - brokuły były w tym badaniu gotowane w wodzie przy pomocy mikrofal, większość strat polifenoli wynikała nie z rozkładu tylko z rozpuszczenia się ich w wodzie, którą wylewano. W czasie tego samego badania stwierdzono też stratę 66% polifenoli podczas gotowania tradycyjnego.[3]
Sami autorzy przyznają zresztą, że te wyniki znacząco odbiegają od uzyskanych w innych badaniach, przykładowo japońscy badacze badający gotowanie cebuli stwierdzili, że między gotowaniem tradycyjnym a mikrofalowym nie ma różnicy dla strat polifenoli [4] a indyjski zespól badający w ten sposób 14 warzyw stwierdził, że straty podczas gotowania na parze i w mikrofali były mniejsze niż podczas gotowania zwykłego.[5]
Tak, że no owszem, bardzo dużą stratę zawartości polifenoli stwierdzono, ale tylko w jednym badaniu. Ponieważ główną przyczyną strat było rozpuszczanie polifenoli w wodzie którą potem odlewano, można się domyśleć, że w przypadku potraw których część stanowią warzywa, i z których nie odlewa się wody, straty będą bardzo małe.
Zmiana kształtu białek
Kolejnym częstym argumentem, jest zmienianie kształtu białek i powodowanie, że stają się nienaturalne. A jeśli coś jest nienaturalne to organizm tego nie poznaje i nie trawi.
Jest to kolejna wieść z kategorii "coś dzwoni ale nie wiadomo w którym uniwersytecie". Owszem, ogrzewanie żywności w mikrofalówce zmienia struktury białek, i to na takie których w naturze nie ma. Tylko że nie jest to nic nadzwyczajnego, zachodzi też podczas smażenia i gotowania. Proces ten nazywa się denaturacją. Przykładowo podczas smażenia jajecznicy rozpuszczalne w wodzie albuminy, będące białkami o cząsteczkach w kształcie kłębków sznurka, rozwijają się i prostują, po czym tworzą siatkę wielu przeplecionych łańcuchów. Taka struktura nie występuje w naturze. Jednak organizm nie ma z nią żadnego problemu. Nasz żołądek nie trudni się rozpoznawaniem struktury białka i testowaniem naturalności konformacji, tylko wytwarza enzymy które tą strukturę naturalną czy nie, niszczą i trawią.
Izomeryzacja aminokwasów
W paru miejscach widziałem, że dla udowodnienia szkodliwego wpływu powoływano się na badania na temat izomeryzacji aminokwasów.[6] Jak to już było tłumaczone we wpisie o witaminie C, w pewnych przypadkach asymetria cząsteczki powoduje, że związki chemiczne mogą posiadać dwie formy, podobne jak lustrzane odbicia ale nie nakładające się.
Takimi związkami są na przykład alfa-aminokwasy budujące białka, ale też często występujące w organizmach swobodnie. Spośród dwóch podobnych form - L i D, w organizmach żywych występują praktycznie tylko aminokwasy L.
No i otóż, jak wykazano podczas ogrzewania mleka w mikrofali, część wolnych aminokwasów ulega izomeryzacji w nienaturalną formę D. Co to powoduje? Wedle artykułów szkodzi i ma uzasadniać szkodliwość mikrofalówek.
Czy D-aminokwasy, które normalnie nie wchodzą w skład białek żywych organizmów, nie występują w przyrodzie i pojawiają się dopiero po nienaturalnym ogrzaniu mikrofalami? Nie.
Nie są zbyt częste, ale pojawiają się w organizmach i żywności wskutek spontanicznej izomeryzacji. Reakcja taka, jak wiele innych, ma pewną określoną szybkość, która zwiększa się po ogrzaniu. I to zupełnie niezależnie od sposobu ogrzewania.
W pewnym badaniu ogrzewano mleko bądź w mikrofalówce lub konwencjonalnie i zbadano zawartość izomerów D kwasu asparaginowego i glutaminowego. Przed ogrzaniem mleko zawierało około 0,4-0,45% tych izomerów, po ogrzaniu zarówno mikrofalowym jak i zwykłym ich zawartość zwiększyła się o 0,25%. Między próbkami ogrzewanymi na różne sposoby przez ten sam czas nie było różnic w zawartości D-izomerów.[7]
W zasadzie z uwagi na to, że mikrofalami można ogrzać mleko szybciej, można by się spodziewać mniejszych poziomów tych izomerów.
Wspomniane izomery D nie są tak znów nienaturalne, skoro dokładne badania wykazują ich niewielkie ilości w różnych produktach naturalnych. W obszernym przeglądzie badań stwierdzono na przykład, że izomery aminokwasów białkowych występują zarówno w mleku surowym jak i pasteryzowanym. Większe ilości pojawiają się w produktach fermentowanych, a więc kefirze, jogurcie i serach, zwłaszcza w serze długo dojrzewającym, wskutek metabolizmu bakterii. Śladowe ilości pojawiają się w mięsie kurczaka i bekonie, i zwiększają po smażeniu, a nawet w chlebie gdzie podpieczenie tosta zwiększa poziom D-aminokwasów prawie dwa razy.[8]
Wykrywa się je także w ludzkim organizmie i podejrzewa, że mogą pełnić pewne funkcje biologiczne, być na przykład neuroprzekaźnikami, trudno więc straszyć ich obecnością.
Enzymy
W paru artykułach wspomniano o niszczeniu przez mikrofale enzymów z jedzenia. To prawda, ale przyczyną jest samo podgrzanie. Enzymy są białkami a wysoka temperatura zmienia ich strukturę i je unieczynnia. Nie ma znaczenia w jaki sposób odbywa się ogrzanie.
Nitrozoaminy
Nitrozoaminy to rakotwórcze produkty reakcji zachodzących w wysokiej temperaturze między aminami i azotynami. Pojawiają się w przetworzonym mięsie podczas pieczenia i smażenia. Artykuły o mikrofalówkach często twierdzą, że podczas ogrzewania w nich tworzy się konkretnie d-nitrozodietanoloamina (NDMA), trudno powiedzieć czemu akurat ta. Są badania na temat powstawania nitrozoamin w ogóle. Na przykład porównując boczek pieczony w mikrofali ze smażonym na patelni, stwierdzono powstawanie nitrozoamin w obu, w tym smażonym w większej ilości.[9]
W badaniu zawartości NDMA w koreańskich owocach morza ogrzewanych na sześć różnych sposobów, stwierdzono że najwyższe poziomy tej substancji powstawały podczas ogrzewania na grillu na węgiel drzewny, a najmniejsze przy ogrzaniu w mikrofalówce i gotowaniu w ciśnieniowej kuchence parowej.[10]
Inne dziwaczne argumenty
Artykuły o mikrofalówkach często są doprawione dziwacznymi wieściami, które w zasadzie nie stanowią żadnych argumentów, ale mają robić atmosferę. Do najczęściej powtarzanych należy wiadomość że ZSRR zakazało domowych mikrofalówek ze względu na dbanie o zdrowie obywateli, tylko nie wiadomo kiedy - daty wahają się od lat 50 do lat 80. Czasem pojawia się twierdzenie, że wynaleźli ją Naziści.
Inną często przytaczaną opowieścią jest śmierć pacjenta któremu przetoczono krew, wcześniej podgrzaną w mikrofalówce, oczywiście wskutek szkodliwego wpływu mikrofal na krew. Taka historia faktycznie miała miejsce w 1989 roku w stanie Oklahoma w USA. Ale przyczyna śmierci była inna - pielęgniarka miała ogrzać krew przechowywaną w lodówce do temperatury ciała pacjenta. Zamiast użyć standardowej łaźni z ciepłą wodą, użyła mikrofali, określając potrzebny czas na wyczucie. W efekcie krew zamiast ogrzać się do tych około 36 stopni, przegrzała się. Wprawdzie ochłodzono ją ale z powodu za wysokiej temperatury doszło do częściowej hemolizy, czyli pęknięcia czerwonych krwinek. Po wprowadzeniu jej do krążenia pojawiły się skrzepy, będąc przyczyną śmierci pacjentki. W 1995 roku rodzina zmarłej dostała odszkodowanie.[11]
Do tego dochodzą takie dziwne twierdzenia jak gromadzenie się mikrofal w jedzeniu, wodzie a nawet meblach kuchennych (!).
Prawdziwy problem
Prawdziwy problem w żywności z mikrofalówki jest taki, że niezbyt dobrą jakość ma żywność do niej wkładania. Gotowe zestawy do podgrzania to często już na wstępie mocno przetworzona żywność z dużą ilością tłuszczy, małą błonnika i witamin. Nie powinny stanowić podstawowej diety w ciągu dnia.
--------
[1] http://www.ptfarm.pl/pub/File/Bromatologia/2013/3/BR%203-2013%20s.%20241-249.pdf
[2] https://www.ptfarm.pl/pub/File/Bromatologia/2013/3/BR%203-2013%20s.%20250-257.pdf
[3] http://www.ingentaconnect.com/content/jws/jsfa/2003/00000083/00000014/art00018;jsessionid=1smkxaf0ymund.victoria
[4] https://www.ncbi.nlm.nih.gov/pubmed/11349895
[5] http://www.ijfans.com/vol2issue3/9.pdf
[6] https://www.ncbi.nlm.nih.gov/pubmed/1968186
[7] https://www.ncbi.nlm.nih.gov/pubmed/7911811
[8] http://www.acta.sapientia.ro/acta-alim/C2-1/alim2-1.pdf
[9] https://www.ncbi.nlm.nih.gov/pubmed/2307266
[10] http://www.tandfonline.com/doi/abs/10.1080/0265203021000014770
[11] http://wyomcases.courts.state.wy.us/applications/oscn/DeliverDocument.asp?citeID=4387
poniedziałek, 6 marca 2017
Ostatnio w laboratorium (55.)
Ostatnio w ramach specjalizacji z krystalografii próbowałem wykrystalizować i wstępnie zbadać kokryształ glicyna+kwas glutarowy. Akurat z samą krystalizacją nie było zbyt dużego problemu:
Kokryształy to kryształy tworzone przez równocześnie dwie lub więcej substancji tworzących powtarzalny układ w sieci. Zwykle precyzuje się, że różne cząsteczki oddziałują niejonowo, co odróżnia je od soli, oraz że obie substancje tworzą czyste kryształy w warunkach istnienia kokryształu, co odróżnia je od hydratów i części klatratów.
Dla danego typu połączenia substancje składowe zachowują stały stosunek stechiometryczny, na przykład dla kryształu chinhydronu na jedną cząsteczkę hydrochinonu przypada jedna cząsteczka chinonu, z którym tworzy kompleks.
Zachodzenie kokrystalizacji może wynikać bądź z tworzenia nowej struktury, bądź z możliwości wpasowania się jednej, podobnej rozmiarami cząsteczki, w normalną sieć krystaliczną drugiego związku. Obecnie temat jest intensywnie badany na potrzeby farmaceutyki, bowiem kokryształy leków mogą być bardziej trwałe, trudniej topliwe lub wykazywać odmienną rozpuszczalność niż substancja czynna w formie czystej.[1]
W tym przypadku sposób otrzymania był prosty, lecz nie do końca pewny - rozpuściliśmy po prostu w wodzie glicynę i kwas glutarowy w stosunku molowym 1:1, nieco ogrzaliśmy dla odparowania aby otrzymać roztwór przesycony i wylaliśmy niewielką ilość na szklaną szalkę. Składniki wykrystalizowały w formie igiełkowatych kryształków i pozostawało tylko dobrać do badania odpowiedni, oraz trafić na kokryształ, bo kształtem nie wyróżniał się od kryształów glicyny i kwasu glutarowego które także mogły powstać.
Pierwszy zbadany kryształek prawdopodobnie należał do poszukiwanego połączenia ale nie dawał sygnału odpowiedniej jakości aby to potwierdzić - był trochę za duży i oprószony drobniejszymi na powierzchni. Ze względu na rozmiar wiązki promieni rentgenowskich, kryształ powinien być mniejszy niż milimetr, oraz powinien być monokryształem bez spękań i przyrośniętych bliźniaków.
Należało więc poszukać następnego. Odpowiednio wyglądającą igłę przyciąłem manipulując pod mikroskopem pęsetą i skalpelem, aby nie była zbyt duża, i przykleiłem na kropelkę do kapilary na końcu główki goniometru. Tym razem szybkie sprawdzenie pokazało sygnał dość dobrej jakości, ale inny niż oczekiwany. Wyselekcjonowany kryształek okazał się glicyną w odmianie alfa.
Zostało mało czasu, więc wybrałem z szalki mały kryształek, którego nie trzeba było ciąć. Niestety podczas próby nałożenia złamała się szklana kapilara do której przyklejane były kryształy. Ostatecznie postanowiliśmy zaryzykować i kryształek został przyklejony do zachowanego kikuta, trochę grubego, ale jeszcze dostatecznego. Kryształ przykleił się krzywo a w dodatku obok przyczepił się czyjś włos. Nie wyglądało to dobrze:
Jednak wstępny pomiar pokazał, że kryształ jest bardzo dobrej jakości, bez zakłóceń, i ma inną grupę przestrzenną. Dzięki temu mogliśmy sprawdzić parametry komórki krystalicznej w bazie i stwierdzić że jest to... glicyna w formie beta.
Odmiana beta jest metastabilna w normalnych warunkach i zwykle szybko zamienia się w formę alfa. Na zajęciach ze studentami kilka miesięcy wcześniej żadnej grupie nie udało się jej uzyskać, a teraz jak na złość. Ponieważ kończył się czas, dalszą krystalizację odłożyliśmy do następnych zajęć.
----------
[1] http://biuletynfarmacji.wum.edu.pl/1305Sokal/Sokal.html
Kokryształy to kryształy tworzone przez równocześnie dwie lub więcej substancji tworzących powtarzalny układ w sieci. Zwykle precyzuje się, że różne cząsteczki oddziałują niejonowo, co odróżnia je od soli, oraz że obie substancje tworzą czyste kryształy w warunkach istnienia kokryształu, co odróżnia je od hydratów i części klatratów.
Dla danego typu połączenia substancje składowe zachowują stały stosunek stechiometryczny, na przykład dla kryształu chinhydronu na jedną cząsteczkę hydrochinonu przypada jedna cząsteczka chinonu, z którym tworzy kompleks.
Zachodzenie kokrystalizacji może wynikać bądź z tworzenia nowej struktury, bądź z możliwości wpasowania się jednej, podobnej rozmiarami cząsteczki, w normalną sieć krystaliczną drugiego związku. Obecnie temat jest intensywnie badany na potrzeby farmaceutyki, bowiem kokryształy leków mogą być bardziej trwałe, trudniej topliwe lub wykazywać odmienną rozpuszczalność niż substancja czynna w formie czystej.[1]
W tym przypadku sposób otrzymania był prosty, lecz nie do końca pewny - rozpuściliśmy po prostu w wodzie glicynę i kwas glutarowy w stosunku molowym 1:1, nieco ogrzaliśmy dla odparowania aby otrzymać roztwór przesycony i wylaliśmy niewielką ilość na szklaną szalkę. Składniki wykrystalizowały w formie igiełkowatych kryształków i pozostawało tylko dobrać do badania odpowiedni, oraz trafić na kokryształ, bo kształtem nie wyróżniał się od kryształów glicyny i kwasu glutarowego które także mogły powstać.
Pierwszy zbadany kryształek prawdopodobnie należał do poszukiwanego połączenia ale nie dawał sygnału odpowiedniej jakości aby to potwierdzić - był trochę za duży i oprószony drobniejszymi na powierzchni. Ze względu na rozmiar wiązki promieni rentgenowskich, kryształ powinien być mniejszy niż milimetr, oraz powinien być monokryształem bez spękań i przyrośniętych bliźniaków.
Należało więc poszukać następnego. Odpowiednio wyglądającą igłę przyciąłem manipulując pod mikroskopem pęsetą i skalpelem, aby nie była zbyt duża, i przykleiłem na kropelkę do kapilary na końcu główki goniometru. Tym razem szybkie sprawdzenie pokazało sygnał dość dobrej jakości, ale inny niż oczekiwany. Wyselekcjonowany kryształek okazał się glicyną w odmianie alfa.
Zostało mało czasu, więc wybrałem z szalki mały kryształek, którego nie trzeba było ciąć. Niestety podczas próby nałożenia złamała się szklana kapilara do której przyklejane były kryształy. Ostatecznie postanowiliśmy zaryzykować i kryształek został przyklejony do zachowanego kikuta, trochę grubego, ale jeszcze dostatecznego. Kryształ przykleił się krzywo a w dodatku obok przyczepił się czyjś włos. Nie wyglądało to dobrze:
Jednak wstępny pomiar pokazał, że kryształ jest bardzo dobrej jakości, bez zakłóceń, i ma inną grupę przestrzenną. Dzięki temu mogliśmy sprawdzić parametry komórki krystalicznej w bazie i stwierdzić że jest to... glicyna w formie beta.
Odmiana beta jest metastabilna w normalnych warunkach i zwykle szybko zamienia się w formę alfa. Na zajęciach ze studentami kilka miesięcy wcześniej żadnej grupie nie udało się jej uzyskać, a teraz jak na złość. Ponieważ kończył się czas, dalszą krystalizację odłożyliśmy do następnych zajęć.
----------
[1] http://biuletynfarmacji.wum.edu.pl/1305Sokal/Sokal.html
niedziela, 5 lutego 2017
Najciekawsze odkrycia chemiczne w 2016 roku
Co w minionym roku chemicy dokonali najciekawszego, wartego uwagi czy choćby nietypowego? Lista odkryć o których nie pisałem w poprzednich wieściach, opracowana częściowo na podstawie tego co zapamiętałem, a częściowo na podstawie innych takich podsumowań zauważonych na zagranicznych portalach (linki na końcu artykułu). Nie pojawia się tu uznanie odkryć i nazwanie czterech nowych pierwiastków, bo już o tym pisałem i nie dotyczyło to odkryć z tego roku. Podobnie jest z tegoroczną nagrodą Nobla, ale tutaj artykuł o niej jeszcze czeka na napisanie.
Najbardziej polarny związek organiczny
Polarność to cecha cząsteczek mówiąca o nierównym rozłożeniu ładunku elektrycznego. Atomy tworzące cząsteczki otoczone są przez elektrony, te jednak są dość ruchliwe. Jeśli w cząsteczce pojawią się rozłożone niesymetrycznie atomy o bardzo różnej elektroujemności (zdolności do przyciągania elektronów), lub grupy z różnych przyczyn odpychające lub przeciągające elektrony, to cząsteczka taka nabierze momentu dipolowego, pokazującego która strona cząsteczki jest nieco bardziej dodatnia a która nieco bardziej ujemna.
Takie polarne właściwości ma choćby woda, składająca się z silnie elektroujemnego tlenu po jednej stronie i słabo elektroujemnych wodorów do drugiej stronie. dzięki tej właściwości woda może łatwiej rozpuszczać sole mineralne i wiele polarnych związków organicznych.
Moment dipolowy jest własnością wektorową, drobne oddziaływania różnych części cząsteczki sumują się do momentu ogólnego.
Silny moment dipolowy posiadają cząsteczki ulegające jonizacji, a więc aniony kwasów karboksylowych, kationy fosfoniowe a szczególnie posiadające fragment anionowy i fragment kationowy betainy. Jednak w opisanym nie tak dawno przypadku wyjątkowo silne oddziaływanie udało się otrzymać dla cząsteczki elektrycznie obojętnej.
Jest to w sumie dość prosty związek 5,5-diamino-1,2,3,4-tatracarbonitrylobenzen , benzen z różnymi podstawnikami - cztery grupy nitrylowe po jednej stronie i dwie aminowe po drugiej. Efekty elektronowe powodują, że grupy aminowe ściągają w swoją stronę elektrony, zaś grupy nitrylowe odpychają. Wskutek dodania się wektorów polaryzacji tych sześciu leżących na jednej płaszczyźnie grup tworzy się moment dipolowy, którego zmierzona wartość osiągnęła 14,1 D. [1] To nawet więcej niż wartość dla niektórych soli nieorganicznych w stanie gazowym. Dla porównania dla cząsteczki wody moment ten ma wartość 1,85 D
Zaproponowano już jednak cząsteczki o potencjale na jeszcze większą polarność, więc rekord jest raczej zagrożony. [2]
Najmocniejsza zasada organiczna
Kolejny rekord odnosi się do innej właściwości cząsteczek organicznych - skłonności do wiązania kationu wodorowego. Związki które chętnie proton oddają, to kwasy, związki które chętnie go przyjmują, to zasady. Niedawno opublikowane obliczenia pokazały, że dianion otro-dietynylobenzenu przyjmuje protony najchętniej, z energią 1834 kJ/mol.[3]
Sześciowiązalny węgiel
Nic tak bardzo nie cieszy chemików, jak odkrycie że coś uznawanego dawniej za pewnik, nim nie jest. I tak jest w tym przypadku.
Heksametylobenzen to dość prosty związek organiczny - benzen zupełnie podstawiony grupami metylowymi. W latach 70. podczas badań nad jego aktywnością zwrócono uwagę na szczególną formę - potraktowanie związku "kwasem magicznym", mieszaniną kwasu fluorosulfonowego i fluorku antymonu o bardzo dużej mocy, spowodowało powstanie dość trwałego dikationu który zachował właściwości aromatyczne, mimo że wydawało się to niemożliwe. Aby to wyjaśnić zaproponowano kilka struktur kationu, wśród nich ekstremalną w formie piramidy pentagonalnej, ale ta wydawała się niemożliwa. Dopiero niedawno udało się uzyskać kryształ soli tego dikationu i zbadać strukturę metodami rentgenowskimi. Dokładne pomiary potwierdziły, że z pozoru nieprawdopodobna propozycja jest prawdziwa.
Po zjonizowaniu cząsteczka ulega przearanżowaniu w formę z jednym pierścieniem pięciokątnym, pięcioma grupami metylowymi po bokach. Jeden węgiel z dawnego pierścienia jest połączony z kolejną grupą metylową i z wszystkimi atomami pierścienia po jednym wiązaniu.
W czym problem? Atomy tworzą wiązania poprzez uwspólnienie elektronów z zewnętrznej, niezapełnionej powłoki, po jednym od każdego, dwa na jedno wiązanie, dążąc do trwalszego energetycznie układu ośmiu elektronów w otoczeniu. Obojętnemu atomowi węgla brakuje do tego stanu 4 elektronów, toteż tworzy maksymalnie 4 wiązania. Wprawdzie znane były związki hiperwalencyjne dla niektórych pierwiastków, gdzie atom tworzył więcej wiązań niż mu starczyło elektronów ale odkrycie, że może je tworzyć też węgiel było dość zaskakujące. Jak na niemetale ma stosunkowo wysoką elektroujemność co powinno przeszkadzać takim połączeniom. Czterowiązalny węgiel to jedno z podstawowych założeń w chemii organicznej.
Prawdopodobnie wiązania są w tym przypadku utworzone poprzez utworzenie orbitalu wielocentrowego, a więc będącego "wiązaniem" łączącym jedną parą elektronową więcej jak dwa atomy, w efekcie węgiel na wierzchołku wprawdzie jest powiązany z sześcioma innymi, ale uzyskuje oktet.[4]
Lek na zatrucie czadem
Tlenek węgla i zatrucia nim kiedyś już omawiałem (link). Wdychany łączy się z hemoglobiną czerwonych krwinek i wypiera z nich tlen, w dodatku połączenie to jest bardzo trwałe, przez co zatruta krwinka nie może już przenosić tlenu. Wraz z kolejnymi wdechami coraz większa ilość krwi ulega zatruciu, zaś człowiek traci przytomność i umiera z powodu niedotlenienia. Ponieważ czad jest bezwonny a niedotlenienie póki jest lekkie nie wywołuje alarmujących objawów, zatrucia nim stają się co roku przyczyną tysięcy zgonów.
Odratowanie częściowo zatrutego jest trudne, najczęściej polega na podawaniu tlenu pod zwiększonym ciśnieniem, czasem próbuje się przetaczania krwi. Dlatego odkrycie, że istnieć może bardziej bezpośrednio działające antidotum, jest bardzo ważne.
Mark Bladwin badał właściwości neuroglobiny, związku podobnego do hemoglobiny występującego w mózgu, mającego pomagać w natlenianiu neuronów Stwierdził podczas analiz, że neuroglobina bardzo silnie wiąże się także z tlenkiem węgla, i to wręcz silniej niż jej kuzynka z krwinek. Dla przebiegu zatrucia miało to o tyle istotne znaczenie, że wskazywało na znacznie silniejszy wpływ nawet małych dawek na mózg, niż na resztę organów. Możliwe, że utrzymywanie się w mózgu tego trwałego połączenia odpowiada za późne neurologiczne objawy zatrucia.
Potem jednak Bladwin skontaktował się z badaczami szukającymi związku, który mógłby usuwać czad z krwi, i zaproponował użycie właśnie tej proteiny. Idea była dość prosta - gdy zatruta hemoglobina z krwinki zetknie się z neuroglobiną, która tworzy z tlenkiem połączenie jeszcze chętniej, nastąpi między nimi wymiana. Neuroglobina utworzy bardzo trwały kompleks z czadem, a hemoglobina z krwinki zostanie odblokowana i zacznie normalnie przenosić tlen.
Pierwsze próby na zwierzętach były bardzo obiecujące, toteż wykorzystano biotechnologię testując wersje neuroglobiny z drobnymi mutacjami. Po wielu próbach i dalszej optymalizacji otrzymano odmianę Ngb H64Q wiążącą się z tlenkiem węgla 500 razy mocniej niż hemoglobina. Podanie jej dożylnie myszom narażonym na śmiertelną dawkę czadu pozwoliło na uratowanie 86% z nich.[5]
Jedwabniki karmione grafenem wytwarzają supernić
To doniesienie brzmi tak dziwacznie, że wciąż czekam czy nie okaże się przemyślnym żartem. Jedwabniki nakarmione liśćmi morwy z dodatkiem węglowych nanorurek i grafenu, wytworzyły jedwab bardziej wytrzymały od naturalnego. Prawdopodobnie cząsteczki białka utworzyły na powierzchni węgla bardziej zbite struktury warstwowe podobne do beta-harmonijki, co zwiększyło ich wytrzymałość.
Po zwęgleniu takiej przędzy powstawało włókno węglowe o zwiększonej przewodności elektrycznej, dlatego dość w sumie prosta technika może znaleźć zastosowanie na przykład do budowy węglowych elektrod.[6]
Chiralne cząstki w kosmosie.
Życie jest chiralne. Organizmy żywe składają się w dużym stopniu ze związków mających tą właściwość, iż ich cząsteczki mogą tworzyć dwie odmiany przestrzenne, nie identyczne lecz podobne jak lustrzane odbicia. Takimi cząsteczkami są aminokwasy, całe białka czy DNA. Co jednak najbardziej interesujące, spośród dwóch lustrzanych form w organizmach żywych występuje tylko jedna - aminokwasy budujące wszystkie białka organizmu mają konfigurację L, izomery w odmianie D są w naturze rzadkością.
Lustrzane izomery aminokwasów niczym się nie różnią pod względem trwałości czy reaktywności, a ponieważ w reakcjach niebiologicznej syntezy zwykle powstaje mieszanina po równo obu izomerów, powstaje pytanie, czemu ziemskie organizmy ostatecznie wykorzystały tylko jedną z wersji tych cząsteczek? Jedną z propozycji jest założenie, że chiralne cząsteczki z nadmiarem jednej z form były obecne w obłoku z którego powstał układ słoneczny, w związku z czym gdy na Ziemi powstało życie, w praoceanie istniała już przewaga związków o jednej konfiguracji. Z kolei nadmiar jednego z izomerów w pierwotnym obłoku miałby wynikać z oświetlenia go błyskiem promieniowania spolaryzowanego kołowo tak, że cząsteczki o różnej konfiguracji a zatem i różnej czynności optycznej, w różnym stopniu pochłaniały energię i w różnym stopniu się rozkładały.
Aby to potwierdzić należałoby najpierw potwierdzić, że w kosmosie istnieją chiralne cząsteczki, a potem że zachodzi nierównowaga między zawartością lustrzanych form L i D. To pierwsze udało się w minionym roku - w obłoku pyłu i gazu Sagittarius B Północny w pobliżu centrum naszej galaktyki, wykryto spektroskopowo sygnał pochodzący od tlenku propylenu, będący takim właśnie chiralnym związkiem.[7]
Karbinowe nanodruty
Były już nanorurki, fullereny i grafen. Czas więc na następną odmianę węgla - karbiny. Chodzi o cząsteczki będące w zasadzie spolimeryzowanym acetylenem, z naprzemiennym układem wiązań pojedynczych i potrójnych (choć ze względu na delokalizację można też opisać je jako łańcuch atomów węgla połączonych wiązaniami podwójnymi).
Przewidziany teoretycznie materiał powinien mieć potencjalnie interesujące właściwości - niezwykle wysoką właściwą wytrzymałość na zerwanie, sztywność większą niż diament, dobre przewodnictwo elektryczne i cieplne. Problemem było natomiast jego otrzymanie - dotychczasowe techniki oparte o redukcję acetylenków metali czy alkenów zwykle prowadziły do otrzymania krótkich odcinków, zakończonych dużymi grupami innego rodzaju, posplatanych i posklejanych na różne sposoby. Jeśli jakiś zespół wymyślił metodę kontrolowanego otrzymania nici 40-50 atomowej, to już tym to sukces.
Dlatego ostatnie odkrycie jest potężnym skokiem technologicznym - przy pomocy odpowiednio dobranych warunków udało się otrzymać węglowe nanorurki z "wkładem" z łańcuchów karbinowych o długości do 6000 atomów. [8]
-------
* Chemistry & Engeenering 10 najbardziej poczytnych artykułów 2016 roku
* Compound Interest Biggest chemistry stories
[1] J. Wudarczyk et. al. Hexasubstituted Benzenes with Ultrastrong Dipole Moments, Angewandte Chemie International Edition, vol. 55, pp. 3220-3223, 2016.
[2] http://www.rzepa.net/blog/?p=17205
[3] Leo Radom et.al. Preparation of an ion with the highest calculated proton affinity: ortho-diethynylbenzene dianion, Chem. Sci., 2016,7, 6245-6250
[4] Moritz Malischewski, K. Seppelt "Crystal Structure Determination of the Pentagonal-Pyramidal Hexamethyl benzene Dication", Angew. Chem. Int.Ed. 56 (1): 368–370.
[5] Mark T. Bladwin et.al. Five-coordinate H64Q neuroglobin as a ligand-trap antidote for carbon monoxide poisoning, Science Translational Medicine 8, 368, pp. 368-173
[6] Qi Wang et al. Feeding Single-Walled Carbon Nanotubes or Graphene to Silkworms for Reinforced Silk Fibers, Nano Letters (2016) 16 (10), pp 6695–6700
[7] B McGuire et al, Discovery of the interstellar chiral molecule propylene oxide (CH3CHCH2O)
Science, 2016, 352, 1449
[8] Thomas Pichler et al. Confined linear carbon chains as a route to bulk carbyne, Nature Materials,15, 634–639
Najbardziej polarny związek organiczny
Polarność to cecha cząsteczek mówiąca o nierównym rozłożeniu ładunku elektrycznego. Atomy tworzące cząsteczki otoczone są przez elektrony, te jednak są dość ruchliwe. Jeśli w cząsteczce pojawią się rozłożone niesymetrycznie atomy o bardzo różnej elektroujemności (zdolności do przyciągania elektronów), lub grupy z różnych przyczyn odpychające lub przeciągające elektrony, to cząsteczka taka nabierze momentu dipolowego, pokazującego która strona cząsteczki jest nieco bardziej dodatnia a która nieco bardziej ujemna.
Takie polarne właściwości ma choćby woda, składająca się z silnie elektroujemnego tlenu po jednej stronie i słabo elektroujemnych wodorów do drugiej stronie. dzięki tej właściwości woda może łatwiej rozpuszczać sole mineralne i wiele polarnych związków organicznych.
Moment dipolowy jest własnością wektorową, drobne oddziaływania różnych części cząsteczki sumują się do momentu ogólnego.
Silny moment dipolowy posiadają cząsteczki ulegające jonizacji, a więc aniony kwasów karboksylowych, kationy fosfoniowe a szczególnie posiadające fragment anionowy i fragment kationowy betainy. Jednak w opisanym nie tak dawno przypadku wyjątkowo silne oddziaływanie udało się otrzymać dla cząsteczki elektrycznie obojętnej.
Jest to w sumie dość prosty związek 5,5-diamino-1,2,3,4-tatracarbonitrylobenzen , benzen z różnymi podstawnikami - cztery grupy nitrylowe po jednej stronie i dwie aminowe po drugiej. Efekty elektronowe powodują, że grupy aminowe ściągają w swoją stronę elektrony, zaś grupy nitrylowe odpychają. Wskutek dodania się wektorów polaryzacji tych sześciu leżących na jednej płaszczyźnie grup tworzy się moment dipolowy, którego zmierzona wartość osiągnęła 14,1 D. [1] To nawet więcej niż wartość dla niektórych soli nieorganicznych w stanie gazowym. Dla porównania dla cząsteczki wody moment ten ma wartość 1,85 D
Zaproponowano już jednak cząsteczki o potencjale na jeszcze większą polarność, więc rekord jest raczej zagrożony. [2]
Najmocniejsza zasada organiczna
Kolejny rekord odnosi się do innej właściwości cząsteczek organicznych - skłonności do wiązania kationu wodorowego. Związki które chętnie proton oddają, to kwasy, związki które chętnie go przyjmują, to zasady. Niedawno opublikowane obliczenia pokazały, że dianion otro-dietynylobenzenu przyjmuje protony najchętniej, z energią 1834 kJ/mol.[3]
Sześciowiązalny węgiel
Nic tak bardzo nie cieszy chemików, jak odkrycie że coś uznawanego dawniej za pewnik, nim nie jest. I tak jest w tym przypadku.
Heksametylobenzen to dość prosty związek organiczny - benzen zupełnie podstawiony grupami metylowymi. W latach 70. podczas badań nad jego aktywnością zwrócono uwagę na szczególną formę - potraktowanie związku "kwasem magicznym", mieszaniną kwasu fluorosulfonowego i fluorku antymonu o bardzo dużej mocy, spowodowało powstanie dość trwałego dikationu który zachował właściwości aromatyczne, mimo że wydawało się to niemożliwe. Aby to wyjaśnić zaproponowano kilka struktur kationu, wśród nich ekstremalną w formie piramidy pentagonalnej, ale ta wydawała się niemożliwa. Dopiero niedawno udało się uzyskać kryształ soli tego dikationu i zbadać strukturę metodami rentgenowskimi. Dokładne pomiary potwierdziły, że z pozoru nieprawdopodobna propozycja jest prawdziwa.
Po zjonizowaniu cząsteczka ulega przearanżowaniu w formę z jednym pierścieniem pięciokątnym, pięcioma grupami metylowymi po bokach. Jeden węgiel z dawnego pierścienia jest połączony z kolejną grupą metylową i z wszystkimi atomami pierścienia po jednym wiązaniu.
W czym problem? Atomy tworzą wiązania poprzez uwspólnienie elektronów z zewnętrznej, niezapełnionej powłoki, po jednym od każdego, dwa na jedno wiązanie, dążąc do trwalszego energetycznie układu ośmiu elektronów w otoczeniu. Obojętnemu atomowi węgla brakuje do tego stanu 4 elektronów, toteż tworzy maksymalnie 4 wiązania. Wprawdzie znane były związki hiperwalencyjne dla niektórych pierwiastków, gdzie atom tworzył więcej wiązań niż mu starczyło elektronów ale odkrycie, że może je tworzyć też węgiel było dość zaskakujące. Jak na niemetale ma stosunkowo wysoką elektroujemność co powinno przeszkadzać takim połączeniom. Czterowiązalny węgiel to jedno z podstawowych założeń w chemii organicznej.
Prawdopodobnie wiązania są w tym przypadku utworzone poprzez utworzenie orbitalu wielocentrowego, a więc będącego "wiązaniem" łączącym jedną parą elektronową więcej jak dwa atomy, w efekcie węgiel na wierzchołku wprawdzie jest powiązany z sześcioma innymi, ale uzyskuje oktet.[4]
Lek na zatrucie czadem
Tlenek węgla i zatrucia nim kiedyś już omawiałem (link). Wdychany łączy się z hemoglobiną czerwonych krwinek i wypiera z nich tlen, w dodatku połączenie to jest bardzo trwałe, przez co zatruta krwinka nie może już przenosić tlenu. Wraz z kolejnymi wdechami coraz większa ilość krwi ulega zatruciu, zaś człowiek traci przytomność i umiera z powodu niedotlenienia. Ponieważ czad jest bezwonny a niedotlenienie póki jest lekkie nie wywołuje alarmujących objawów, zatrucia nim stają się co roku przyczyną tysięcy zgonów.
Odratowanie częściowo zatrutego jest trudne, najczęściej polega na podawaniu tlenu pod zwiększonym ciśnieniem, czasem próbuje się przetaczania krwi. Dlatego odkrycie, że istnieć może bardziej bezpośrednio działające antidotum, jest bardzo ważne.
Mark Bladwin badał właściwości neuroglobiny, związku podobnego do hemoglobiny występującego w mózgu, mającego pomagać w natlenianiu neuronów Stwierdził podczas analiz, że neuroglobina bardzo silnie wiąże się także z tlenkiem węgla, i to wręcz silniej niż jej kuzynka z krwinek. Dla przebiegu zatrucia miało to o tyle istotne znaczenie, że wskazywało na znacznie silniejszy wpływ nawet małych dawek na mózg, niż na resztę organów. Możliwe, że utrzymywanie się w mózgu tego trwałego połączenia odpowiada za późne neurologiczne objawy zatrucia.
Potem jednak Bladwin skontaktował się z badaczami szukającymi związku, który mógłby usuwać czad z krwi, i zaproponował użycie właśnie tej proteiny. Idea była dość prosta - gdy zatruta hemoglobina z krwinki zetknie się z neuroglobiną, która tworzy z tlenkiem połączenie jeszcze chętniej, nastąpi między nimi wymiana. Neuroglobina utworzy bardzo trwały kompleks z czadem, a hemoglobina z krwinki zostanie odblokowana i zacznie normalnie przenosić tlen.
Pierwsze próby na zwierzętach były bardzo obiecujące, toteż wykorzystano biotechnologię testując wersje neuroglobiny z drobnymi mutacjami. Po wielu próbach i dalszej optymalizacji otrzymano odmianę Ngb H64Q wiążącą się z tlenkiem węgla 500 razy mocniej niż hemoglobina. Podanie jej dożylnie myszom narażonym na śmiertelną dawkę czadu pozwoliło na uratowanie 86% z nich.[5]
Jedwabniki karmione grafenem wytwarzają supernić
To doniesienie brzmi tak dziwacznie, że wciąż czekam czy nie okaże się przemyślnym żartem. Jedwabniki nakarmione liśćmi morwy z dodatkiem węglowych nanorurek i grafenu, wytworzyły jedwab bardziej wytrzymały od naturalnego. Prawdopodobnie cząsteczki białka utworzyły na powierzchni węgla bardziej zbite struktury warstwowe podobne do beta-harmonijki, co zwiększyło ich wytrzymałość.
Po zwęgleniu takiej przędzy powstawało włókno węglowe o zwiększonej przewodności elektrycznej, dlatego dość w sumie prosta technika może znaleźć zastosowanie na przykład do budowy węglowych elektrod.[6]
Chiralne cząstki w kosmosie.
Życie jest chiralne. Organizmy żywe składają się w dużym stopniu ze związków mających tą właściwość, iż ich cząsteczki mogą tworzyć dwie odmiany przestrzenne, nie identyczne lecz podobne jak lustrzane odbicia. Takimi cząsteczkami są aminokwasy, całe białka czy DNA. Co jednak najbardziej interesujące, spośród dwóch lustrzanych form w organizmach żywych występuje tylko jedna - aminokwasy budujące wszystkie białka organizmu mają konfigurację L, izomery w odmianie D są w naturze rzadkością.
Lustrzane izomery aminokwasów niczym się nie różnią pod względem trwałości czy reaktywności, a ponieważ w reakcjach niebiologicznej syntezy zwykle powstaje mieszanina po równo obu izomerów, powstaje pytanie, czemu ziemskie organizmy ostatecznie wykorzystały tylko jedną z wersji tych cząsteczek? Jedną z propozycji jest założenie, że chiralne cząsteczki z nadmiarem jednej z form były obecne w obłoku z którego powstał układ słoneczny, w związku z czym gdy na Ziemi powstało życie, w praoceanie istniała już przewaga związków o jednej konfiguracji. Z kolei nadmiar jednego z izomerów w pierwotnym obłoku miałby wynikać z oświetlenia go błyskiem promieniowania spolaryzowanego kołowo tak, że cząsteczki o różnej konfiguracji a zatem i różnej czynności optycznej, w różnym stopniu pochłaniały energię i w różnym stopniu się rozkładały.
Aby to potwierdzić należałoby najpierw potwierdzić, że w kosmosie istnieją chiralne cząsteczki, a potem że zachodzi nierównowaga między zawartością lustrzanych form L i D. To pierwsze udało się w minionym roku - w obłoku pyłu i gazu Sagittarius B Północny w pobliżu centrum naszej galaktyki, wykryto spektroskopowo sygnał pochodzący od tlenku propylenu, będący takim właśnie chiralnym związkiem.[7]
Karbinowe nanodruty
Były już nanorurki, fullereny i grafen. Czas więc na następną odmianę węgla - karbiny. Chodzi o cząsteczki będące w zasadzie spolimeryzowanym acetylenem, z naprzemiennym układem wiązań pojedynczych i potrójnych (choć ze względu na delokalizację można też opisać je jako łańcuch atomów węgla połączonych wiązaniami podwójnymi).
Przewidziany teoretycznie materiał powinien mieć potencjalnie interesujące właściwości - niezwykle wysoką właściwą wytrzymałość na zerwanie, sztywność większą niż diament, dobre przewodnictwo elektryczne i cieplne. Problemem było natomiast jego otrzymanie - dotychczasowe techniki oparte o redukcję acetylenków metali czy alkenów zwykle prowadziły do otrzymania krótkich odcinków, zakończonych dużymi grupami innego rodzaju, posplatanych i posklejanych na różne sposoby. Jeśli jakiś zespół wymyślił metodę kontrolowanego otrzymania nici 40-50 atomowej, to już tym to sukces.
Dlatego ostatnie odkrycie jest potężnym skokiem technologicznym - przy pomocy odpowiednio dobranych warunków udało się otrzymać węglowe nanorurki z "wkładem" z łańcuchów karbinowych o długości do 6000 atomów. [8]
-------
* Chemistry & Engeenering 10 najbardziej poczytnych artykułów 2016 roku
* Compound Interest Biggest chemistry stories
[1] J. Wudarczyk et. al. Hexasubstituted Benzenes with Ultrastrong Dipole Moments, Angewandte Chemie International Edition, vol. 55, pp. 3220-3223, 2016.
[2] http://www.rzepa.net/blog/?p=17205
[3] Leo Radom et.al. Preparation of an ion with the highest calculated proton affinity: ortho-diethynylbenzene dianion, Chem. Sci., 2016,7, 6245-6250
[4] Moritz Malischewski, K. Seppelt "Crystal Structure Determination of the Pentagonal-Pyramidal Hexamethyl benzene Dication", Angew. Chem. Int.Ed. 56 (1): 368–370.
[5] Mark T. Bladwin et.al. Five-coordinate H64Q neuroglobin as a ligand-trap antidote for carbon monoxide poisoning, Science Translational Medicine 8, 368, pp. 368-173
[6] Qi Wang et al. Feeding Single-Walled Carbon Nanotubes or Graphene to Silkworms for Reinforced Silk Fibers, Nano Letters (2016) 16 (10), pp 6695–6700
[7] B McGuire et al, Discovery of the interstellar chiral molecule propylene oxide (CH3CHCH2O)
Science, 2016, 352, 1449
[8] Thomas Pichler et al. Confined linear carbon chains as a route to bulk carbyne, Nature Materials,15, 634–639
środa, 1 lutego 2017
Witamina lewa i prawa
Na temat witaminy C krąży bardzo wiele mitów i przekłamań. A ponieważ mają one w dużym stopniu oparcie w chemii, warto jest je tutaj szczegółowo rozjaśnić. Czy zatem może być tak, że witamina może być prawa i lewa? Może i to w dodatku na bardzo różne sposoby.
Kwas askorbinowy to związek szczególny. Jest kofaktorem regulującym działanie wielu enzymów. Pomaga przy produkcji kolagenu, wpływając na stan naczyń krwionośnych i skóry. Jest ważnym przeciwutleniaczem neutralizującym wolne rodniki. A przy tym jest substancją jakiej nasz organizm nie może sam wytwarzać, co zresztą stanowi wśród zwierząt wyjątek. Takie na przykład szczury same go sobie wytwarzają i nigdy nie doznają niedoboru.
Jego brak wywołuje przykre i na dłuższą metę śmiertelne choroby, jak choćby szkorbut, nazywany też obrazowo gnilcem, co zanim poznano jego rolę w żywieniu stanowiło częstą przyczyną zgonów marynarzy, pozbawionych dostępu do świeżej żywności. Nic więc dziwnego, że witamina C została nazwana kwasem a-skorbinowym, to jest antyszkorbutowym.
Człowiek wynalazł kilka prostych sposobów jego syntezy tak, aby otrzymać cząsteczkę o budowie takiej samej jak naturalna. Zwykle surowcem jest cukier glukoza, która zostaje zredukowana wodorem, poddana fermentacji przez bakterie octowe, selektywnie utleniona i odwodniona. W ten sposób, bądź metodami z większym udziałem bakterii, produkuje się ją w ilościach niemal przemysłowych i zużywa głownie jako przeciwutleniacz w żywności, środek zapobiegający brązowieniu mrożonek czy ulepszacz do pieczywa.
Zasadniczo dobrze zbilansowana dieta powinna dostarczać go nam wręcz w nadmiarze, jednak niektórzy wolą go sobie dodatkowo uzupełniać w większych dawkach. I często wpadają w pułapkę marketingu. Specjaliści od suplementów mówią im "Nie kupujcie pigułek w aptece bo w ogóle nie działają, bierzcie wyciąg z X albo tabletki dla których specjalnie potwierdzono że to jest ten właściwy, przypadkiem mamy je w ofercie. Bierz tylko nasze".
Czemu tabletkowa witamina ma nie działać? Bo "prawdziwa" i naturalna jest ta lewoskrętna, więc jeśli na opakowaniu nie zostanie wprost to napisane, to niechybnie tabletki zawierają tą nieczynną prawoskrętną.
Każdy kto ma trochę większe pojęcie o chemii, wie jak zbudowana jest cząsteczka witaminy C i wie o co chodzi z tą skrętnością, czy lewością, uśmieje się słysząc takie rzeczy. Ale niestety przeciętny konsument nie wie. Więc ja mu rzecz krótko wyjaśnię
Asymetria
Asymetria to własność obiektu, która powoduje, że obracając go w przestrzeni, odbijając w wyimaginowanym "lustrze kształtów" czy przekształcając przez punkt nie otrzymamy identycznie wyglądającej bryły. No chyba, że obrócimy go o 360 stopni czy powtórzymy odbicia dwa razy, ale to tak jakbyśmy go z miejsca nie ruszali.
Chemicy już dawno odkryli, że cząsteczki związków chemicznych, będące ułożonymi w przestrzeniami skupiskami atomów, mogą bądź posiadać jakąś symetrię, bądź nie posiadać żadnej, i to właśnie te ostatnie okazały się najciekawsze. Jeśli cząsteczka związku jest asymetryczna, to bardzo często możliwe jest, że mogą istnieć jej dwie formy, podobne do siebie jak lustrzane odbicia ale nie nakładające się na siebie.
Obiektami o takich własnościach z jakimi często mamy do czynienia, są nasze ręce - jedna dłoń jest lustrzanie podobna do drugiej, ale jedna nie nałoży się na kształt drugiej, bo kciuki odchylają się w różne strony. Jeśli złożymy dłonie jak do modlitwy sytuacja będzie podobna, bo w różne strony będą zwrócone ich grzbiety. Z tego powodu matematycy bryły o takich właściwościach, a więc posiadające lustrzanie podobne formy "lewą" i "prawą" jak dłonie, nazwali chiralnymi, od greckiego "chira" to jest ręka. (a wróżenie z dłoni to chiromancja).
Jeśli cząsteczka związku chemicznego nie będzie posiadała elementów symetrii, takich jak środek symetrii, płaszczyzna czy osie inwersyjne, to także i dla niej możliwe będzie dla niej istnienie w dwóch formach, nazywanych izomerami optycznymi. Zazwyczaj dotyczy to związków organicznych, w których atom węgla tworzy cztery wiązania ułożone nie płasko, i wystarczy aby w którymkolwiek z węgli cząsteczki zdarzyło się, że do każdego wiązania będzie przyczepione coś innego.
Aby ten fakt opisać i jakoś odróżniać poza tym we wszystkim identyczne izomery, chemicy stworzyli szereg systemów klasyfikujących
R czy S?
Ten sposób klasyfikacji opiera się na rzeczywistej budowie związku. Aby sprawdzić jaka jest jego konfiguracja, sprowadzamy go do tego właśnie interesującego nas węgla, mającego cztery różne podstawniki, nazywanego asymetrycznym. Podstawnikom tym nadajemy pewne rangi, zależne od stopnia rozbudowania, całkowitej masy atomowej czy obecności cięższych atomów. No i otóż, jeśli ustawimy naszą cząsteczkę tak, że podstawnik najniższej rangi znajdzie się z tyłu, a trzy pozostałe będą skierowane w naszą stronę, to gdy przechodząc od podstawnika ważniejszego do mniej ważnych wykonujemy obrót w prawo, konfiguracja dla tego węgla wynosi R a gdy w lewo wynosi S.
Ten sposób klasyfikacji jest bardzo ścisły, po samej nazwie możemy ustalić jak przestrzennie są poustawiane grupy wokół tego atomu.
W jednej cząsteczce może być zawartych wiele takich atomów, ponieważ zaś każdy ma dwie możliwe konfiguracje, możliwych staje się wiele izomerów. Przykładowo glukoza ma cztery takie atomy o konfiguracji 2R,3S,4R,5R, będąc jednym z 16 możliwych izomerów aldoheksozy. Symetria takich cząsteczek jest bardziej skomplikowana i niekoniecznie chiralna, przykładowo związki w odmianie mezo zawierają asymetryczne atomy węgla ale o przeciwnej konfiguracji, co powoduje że cała cząsteczka nabiera symetrii i nie jest czynna optycznie.
D czy L?
Klasyfikacja D/L jest używana właściwie tylko do cukrów, polialkoholi i aminokwasów, także dla witaminy C. Jest to klasyfikacja względna, w której przypisanie związku do danej kategorii odbywa się poprzez porównanie konfiguracji z pewnym wzorcem.
Tą cząsteczką wzorcową był naturalnie występujący aldehyd glicerynowy, uznany z najprostszy przypadek, składał się bowiem z trzech węgli z czym jeden tylko był asymetryczny. Klasyfikacja odbywa się następująco - ustawiamy naszą cząsteczkę aby łańcuch węglowy był ustawiony pionowo, grupa aldehydowa lub ketonowa znalazła się na górze, a grupy boczne sterczały na boki, będąc zwrócone lekko w naszą stronę (co rysuje się w ten sposób, że ich wiązania wyglądają jak czarne trójkąty):
Jeśli w takim ustawieniu grupa -OH znajdzie się po prawej, to cząsteczkę zaliczymy do szeregu D a jeśli po lewej to do szeregu L. Jeśli nasza cząsteczka zawiera więcej węgli asymetrycznych, wtedy bierzemy pod uwagę tylko ten ostatni na dole.
Jak widzicie jest to klasyfikacja bardzo arbitralna.
+ czy -?
Ostatni sposób klasyfikacji nie jest wprost związany z budową cząsteczki, a bardziej z tym jak oddziałuje ze światłem. Otóż izomery geometryczne związków wpływają na światło spolaryzowane. Jeśli przez fiolkę ze związkiem przepuścimy światło spolaryzowane przy pomocy polaryzatora ustawionego w określonym kierunku, to po przejściu przez związek kierunek polaryzacji światła trochę się przekręci. Poznajemy to po tym, że ustawiając za fiolką drugi polaryzator widzimy że część światła z fiolki jest zatrzymywana i aby uzyskać pełną przepuszczalność, musimy drugi polaryzator trochę obrócić.
Obejrzyjcie świetną demonstrację tego zjawiska dla dwóch izomerów karwonu:
.
I teraz najważniejsze. Uznano, że jeśli płaszczyzna polaryzacji obróciła się w prawo, to mówimy o związku że jest prawoskrętny i przypisujemy mu znaczek plus (+) a jeśli w lewo to jest lewoskrętny i przypisujemy mu znaczek minus (-). Dwa izomery optyczne tej samej substancji skręcają światło spolaryzowane o taki sam kąt w przeciwne strony, dlatego zawsze jeden jest (+) a drugi (-). Ich mieszanina pół na pół jest nieaktywna bo przeciwne oddziaływania się znoszą.
Przy czym nie koniecznie znak skręcalności powiązany jest z konfiguracją R/S czy D/L. Wprawdzie dany określony izomer geometryczny ma zawsze dany określony znak skręcalności, ale różne związki o konfiguracji D czy R mogą skręcać światło spolaryzowane w różne strony. Na przykład D-glukoza jest prawoskrętna a D-fruktoza lewoskrętna.
A jaka jest witamina?
Kwas askorbinowy zawiera dwa węgle asymetryczne, w związku z czym możliwe są dla niego cztery izomery; kwas (R,S)-L-askorbinowy, (S,R)-D-askorbinowy; (S,S)-L-izoaskorbinowy i (R,R)-D-izoaskorbinowy
Aktywność biologiczną witaminy ma tylko jeden z nich, występujący naturalnie kwas (R,S) L-askorbinowy. Pozostałe nie mogą być nazywane witaminami, choć są podobnymi do niej przeciwutleniaczami..
A jak wygląda czynność optyczna? Otóż będący witaminą C naturalny kwas L-askorbinowy jest prawoskrętny. Czyli ma znaczek (+).
Zatem specjaliści od wciskania ludziom suplementów, którzy twierdzą, że witamina C powinna być lewoskrętna, pewnie pomylili się widząc znaczek L mówiący o względnej konfiguracji związku. Który to mówi nam jedynie, że jeśli zapiszemy cząsteczkę związku w określony sposób to grupa -OH na ostatnim węglu asymetrycznym będzie po lewej stronie rysunku, a to nie ma nic do skrętności.
...bo jak nie napisali L to na pewno jest D
Gdy świat alternatywnej medycyny pojął wreszcie istnienie dwóch odmian kwasu askorbinowego, zaczął przekonywać, że z pewnością absolutnie ta tabletkowa witamina, to jest właśnie ta nienaturalna D. Ze jeśli nie napiszą "kwas L-askorbinowy" to znaczy, że to musi być ten drugi. Ci którzy się na to nabierają zamawiają w hurtowniach wielkie wory kwasu L, nie ufając tabletkom, no bo przecież kto wie co sobie producenci napisali.
Dlaczego to bzdura?
Jak to już powyżej napisałem, kwas L-askorbinowy produkuje się z naturalnej glukozy otrzymując właściwą "naturalną" konfigurację. Wobec tego związek jest dosyć tani i dlatego bardziej opłaca się pchać go do tabletek, niż drugi izomer, produkowany w mniejszych ilościach przy pomocy innych, bardziej skomplikowanych metod. Kwas D-askorbinowy nie występuje w naturze a organizmy nie są przystosowane do jego wytwarzania, odpada więc bardzo ułatwiający produkcję mikrobiologiczny etap syntezy. Aby go otrzymać należałoby więc albo użyć drogich katalizatorów albo szeregu przemian dających mieszaninę izomerów, którą następnie należałoby rozdzielać. Ponieważ jednak izomer D nie jest wykorzystywany w medycynie, nikt go specjalnie nie produkuje. Czemu więc tabletki miałyby zawierać nie produkowany, znacznie droższy, nieaktywny izomer, gdy w zasięgu jest produkowany na dużą skalę aktywny L-izomer?
Inna kwestia to dozwolone nazewnictwo obu odmian. Nazwa handlowa "witamina C" oraz nazwa "kwas askorbinowy" są na mocy międzynarodowych przepisów zastrzeżone tylko dla kwasu L-(+)-askorbinowego, takiego jak naturalny. Producent nie może wsadzać w preparat inny stereoizomer i nazwać go witaminą. Ponieważ w świetle przepisów jest to w sumie jasne, producent tabletek nie musi pisać na opakowaniu, że tabletka zawiera kwas L-(+)-(4R,5S)-askorbinowy abyśmy byli pewni, że jest to taka cząsteczka jak naturalna, działająca biologicznie.
ps. 03.02 Dowiedziałem się, że w lutowym numerze Wiedzy i Życia także pojawił się artykuł o witaminie C. Jest dużo obszerniejszy i skupia się głównie na zastosowaniach medycznych ale o skrętności też wspomina. Polecam zajrzeć.
Kwas askorbinowy to związek szczególny. Jest kofaktorem regulującym działanie wielu enzymów. Pomaga przy produkcji kolagenu, wpływając na stan naczyń krwionośnych i skóry. Jest ważnym przeciwutleniaczem neutralizującym wolne rodniki. A przy tym jest substancją jakiej nasz organizm nie może sam wytwarzać, co zresztą stanowi wśród zwierząt wyjątek. Takie na przykład szczury same go sobie wytwarzają i nigdy nie doznają niedoboru.
Jego brak wywołuje przykre i na dłuższą metę śmiertelne choroby, jak choćby szkorbut, nazywany też obrazowo gnilcem, co zanim poznano jego rolę w żywieniu stanowiło częstą przyczyną zgonów marynarzy, pozbawionych dostępu do świeżej żywności. Nic więc dziwnego, że witamina C została nazwana kwasem a-skorbinowym, to jest antyszkorbutowym.
Człowiek wynalazł kilka prostych sposobów jego syntezy tak, aby otrzymać cząsteczkę o budowie takiej samej jak naturalna. Zwykle surowcem jest cukier glukoza, która zostaje zredukowana wodorem, poddana fermentacji przez bakterie octowe, selektywnie utleniona i odwodniona. W ten sposób, bądź metodami z większym udziałem bakterii, produkuje się ją w ilościach niemal przemysłowych i zużywa głownie jako przeciwutleniacz w żywności, środek zapobiegający brązowieniu mrożonek czy ulepszacz do pieczywa.
Zasadniczo dobrze zbilansowana dieta powinna dostarczać go nam wręcz w nadmiarze, jednak niektórzy wolą go sobie dodatkowo uzupełniać w większych dawkach. I często wpadają w pułapkę marketingu. Specjaliści od suplementów mówią im "Nie kupujcie pigułek w aptece bo w ogóle nie działają, bierzcie wyciąg z X albo tabletki dla których specjalnie potwierdzono że to jest ten właściwy, przypadkiem mamy je w ofercie. Bierz tylko nasze".
Czemu tabletkowa witamina ma nie działać? Bo "prawdziwa" i naturalna jest ta lewoskrętna, więc jeśli na opakowaniu nie zostanie wprost to napisane, to niechybnie tabletki zawierają tą nieczynną prawoskrętną.
Każdy kto ma trochę większe pojęcie o chemii, wie jak zbudowana jest cząsteczka witaminy C i wie o co chodzi z tą skrętnością, czy lewością, uśmieje się słysząc takie rzeczy. Ale niestety przeciętny konsument nie wie. Więc ja mu rzecz krótko wyjaśnię
Asymetria
Asymetria to własność obiektu, która powoduje, że obracając go w przestrzeni, odbijając w wyimaginowanym "lustrze kształtów" czy przekształcając przez punkt nie otrzymamy identycznie wyglądającej bryły. No chyba, że obrócimy go o 360 stopni czy powtórzymy odbicia dwa razy, ale to tak jakbyśmy go z miejsca nie ruszali.
Chemicy już dawno odkryli, że cząsteczki związków chemicznych, będące ułożonymi w przestrzeniami skupiskami atomów, mogą bądź posiadać jakąś symetrię, bądź nie posiadać żadnej, i to właśnie te ostatnie okazały się najciekawsze. Jeśli cząsteczka związku jest asymetryczna, to bardzo często możliwe jest, że mogą istnieć jej dwie formy, podobne do siebie jak lustrzane odbicia ale nie nakładające się na siebie.
Obiektami o takich własnościach z jakimi często mamy do czynienia, są nasze ręce - jedna dłoń jest lustrzanie podobna do drugiej, ale jedna nie nałoży się na kształt drugiej, bo kciuki odchylają się w różne strony. Jeśli złożymy dłonie jak do modlitwy sytuacja będzie podobna, bo w różne strony będą zwrócone ich grzbiety. Z tego powodu matematycy bryły o takich właściwościach, a więc posiadające lustrzanie podobne formy "lewą" i "prawą" jak dłonie, nazwali chiralnymi, od greckiego "chira" to jest ręka. (a wróżenie z dłoni to chiromancja).
Jeśli cząsteczka związku chemicznego nie będzie posiadała elementów symetrii, takich jak środek symetrii, płaszczyzna czy osie inwersyjne, to także i dla niej możliwe będzie dla niej istnienie w dwóch formach, nazywanych izomerami optycznymi. Zazwyczaj dotyczy to związków organicznych, w których atom węgla tworzy cztery wiązania ułożone nie płasko, i wystarczy aby w którymkolwiek z węgli cząsteczki zdarzyło się, że do każdego wiązania będzie przyczepione coś innego.
Aby ten fakt opisać i jakoś odróżniać poza tym we wszystkim identyczne izomery, chemicy stworzyli szereg systemów klasyfikujących
R czy S?
Ten sposób klasyfikacji opiera się na rzeczywistej budowie związku. Aby sprawdzić jaka jest jego konfiguracja, sprowadzamy go do tego właśnie interesującego nas węgla, mającego cztery różne podstawniki, nazywanego asymetrycznym. Podstawnikom tym nadajemy pewne rangi, zależne od stopnia rozbudowania, całkowitej masy atomowej czy obecności cięższych atomów. No i otóż, jeśli ustawimy naszą cząsteczkę tak, że podstawnik najniższej rangi znajdzie się z tyłu, a trzy pozostałe będą skierowane w naszą stronę, to gdy przechodząc od podstawnika ważniejszego do mniej ważnych wykonujemy obrót w prawo, konfiguracja dla tego węgla wynosi R a gdy w lewo wynosi S.
Ten sposób klasyfikacji jest bardzo ścisły, po samej nazwie możemy ustalić jak przestrzennie są poustawiane grupy wokół tego atomu.
W jednej cząsteczce może być zawartych wiele takich atomów, ponieważ zaś każdy ma dwie możliwe konfiguracje, możliwych staje się wiele izomerów. Przykładowo glukoza ma cztery takie atomy o konfiguracji 2R,3S,4R,5R, będąc jednym z 16 możliwych izomerów aldoheksozy. Symetria takich cząsteczek jest bardziej skomplikowana i niekoniecznie chiralna, przykładowo związki w odmianie mezo zawierają asymetryczne atomy węgla ale o przeciwnej konfiguracji, co powoduje że cała cząsteczka nabiera symetrii i nie jest czynna optycznie.
D czy L?
Klasyfikacja D/L jest używana właściwie tylko do cukrów, polialkoholi i aminokwasów, także dla witaminy C. Jest to klasyfikacja względna, w której przypisanie związku do danej kategorii odbywa się poprzez porównanie konfiguracji z pewnym wzorcem.
Tą cząsteczką wzorcową był naturalnie występujący aldehyd glicerynowy, uznany z najprostszy przypadek, składał się bowiem z trzech węgli z czym jeden tylko był asymetryczny. Klasyfikacja odbywa się następująco - ustawiamy naszą cząsteczkę aby łańcuch węglowy był ustawiony pionowo, grupa aldehydowa lub ketonowa znalazła się na górze, a grupy boczne sterczały na boki, będąc zwrócone lekko w naszą stronę (co rysuje się w ten sposób, że ich wiązania wyglądają jak czarne trójkąty):
Jeśli w takim ustawieniu grupa -OH znajdzie się po prawej, to cząsteczkę zaliczymy do szeregu D a jeśli po lewej to do szeregu L. Jeśli nasza cząsteczka zawiera więcej węgli asymetrycznych, wtedy bierzemy pod uwagę tylko ten ostatni na dole.
Jak widzicie jest to klasyfikacja bardzo arbitralna.
+ czy -?
Ostatni sposób klasyfikacji nie jest wprost związany z budową cząsteczki, a bardziej z tym jak oddziałuje ze światłem. Otóż izomery geometryczne związków wpływają na światło spolaryzowane. Jeśli przez fiolkę ze związkiem przepuścimy światło spolaryzowane przy pomocy polaryzatora ustawionego w określonym kierunku, to po przejściu przez związek kierunek polaryzacji światła trochę się przekręci. Poznajemy to po tym, że ustawiając za fiolką drugi polaryzator widzimy że część światła z fiolki jest zatrzymywana i aby uzyskać pełną przepuszczalność, musimy drugi polaryzator trochę obrócić.
Obejrzyjcie świetną demonstrację tego zjawiska dla dwóch izomerów karwonu:
.
I teraz najważniejsze. Uznano, że jeśli płaszczyzna polaryzacji obróciła się w prawo, to mówimy o związku że jest prawoskrętny i przypisujemy mu znaczek plus (+) a jeśli w lewo to jest lewoskrętny i przypisujemy mu znaczek minus (-). Dwa izomery optyczne tej samej substancji skręcają światło spolaryzowane o taki sam kąt w przeciwne strony, dlatego zawsze jeden jest (+) a drugi (-). Ich mieszanina pół na pół jest nieaktywna bo przeciwne oddziaływania się znoszą.
Przy czym nie koniecznie znak skręcalności powiązany jest z konfiguracją R/S czy D/L. Wprawdzie dany określony izomer geometryczny ma zawsze dany określony znak skręcalności, ale różne związki o konfiguracji D czy R mogą skręcać światło spolaryzowane w różne strony. Na przykład D-glukoza jest prawoskrętna a D-fruktoza lewoskrętna.
A jaka jest witamina?
Kwas askorbinowy zawiera dwa węgle asymetryczne, w związku z czym możliwe są dla niego cztery izomery; kwas (R,S)-L-askorbinowy, (S,R)-D-askorbinowy; (S,S)-L-izoaskorbinowy i (R,R)-D-izoaskorbinowy
Aktywność biologiczną witaminy ma tylko jeden z nich, występujący naturalnie kwas (R,S) L-askorbinowy. Pozostałe nie mogą być nazywane witaminami, choć są podobnymi do niej przeciwutleniaczami..
A jak wygląda czynność optyczna? Otóż będący witaminą C naturalny kwas L-askorbinowy jest prawoskrętny. Czyli ma znaczek (+).
Zatem specjaliści od wciskania ludziom suplementów, którzy twierdzą, że witamina C powinna być lewoskrętna, pewnie pomylili się widząc znaczek L mówiący o względnej konfiguracji związku. Który to mówi nam jedynie, że jeśli zapiszemy cząsteczkę związku w określony sposób to grupa -OH na ostatnim węglu asymetrycznym będzie po lewej stronie rysunku, a to nie ma nic do skrętności.
...bo jak nie napisali L to na pewno jest D
Gdy świat alternatywnej medycyny pojął wreszcie istnienie dwóch odmian kwasu askorbinowego, zaczął przekonywać, że z pewnością absolutnie ta tabletkowa witamina, to jest właśnie ta nienaturalna D. Ze jeśli nie napiszą "kwas L-askorbinowy" to znaczy, że to musi być ten drugi. Ci którzy się na to nabierają zamawiają w hurtowniach wielkie wory kwasu L, nie ufając tabletkom, no bo przecież kto wie co sobie producenci napisali.
Dlaczego to bzdura?
Jak to już powyżej napisałem, kwas L-askorbinowy produkuje się z naturalnej glukozy otrzymując właściwą "naturalną" konfigurację. Wobec tego związek jest dosyć tani i dlatego bardziej opłaca się pchać go do tabletek, niż drugi izomer, produkowany w mniejszych ilościach przy pomocy innych, bardziej skomplikowanych metod. Kwas D-askorbinowy nie występuje w naturze a organizmy nie są przystosowane do jego wytwarzania, odpada więc bardzo ułatwiający produkcję mikrobiologiczny etap syntezy. Aby go otrzymać należałoby więc albo użyć drogich katalizatorów albo szeregu przemian dających mieszaninę izomerów, którą następnie należałoby rozdzielać. Ponieważ jednak izomer D nie jest wykorzystywany w medycynie, nikt go specjalnie nie produkuje. Czemu więc tabletki miałyby zawierać nie produkowany, znacznie droższy, nieaktywny izomer, gdy w zasięgu jest produkowany na dużą skalę aktywny L-izomer?
Inna kwestia to dozwolone nazewnictwo obu odmian. Nazwa handlowa "witamina C" oraz nazwa "kwas askorbinowy" są na mocy międzynarodowych przepisów zastrzeżone tylko dla kwasu L-(+)-askorbinowego, takiego jak naturalny. Producent nie może wsadzać w preparat inny stereoizomer i nazwać go witaminą. Ponieważ w świetle przepisów jest to w sumie jasne, producent tabletek nie musi pisać na opakowaniu, że tabletka zawiera kwas L-(+)-(4R,5S)-askorbinowy abyśmy byli pewni, że jest to taka cząsteczka jak naturalna, działająca biologicznie.
ps. 03.02 Dowiedziałem się, że w lutowym numerze Wiedzy i Życia także pojawił się artykuł o witaminie C. Jest dużo obszerniejszy i skupia się głównie na zastosowaniach medycznych ale o skrętności też wspomina. Polecam zajrzeć.
środa, 11 stycznia 2017
Ostatnio w laboratorium (54.)
Kryształy białka lizozymu, otrzymane metodą wiszącej kropli:
Lizozym to enzym bakteriobójczy, powodujący rozkład glikoprotein w ścianie komórkowej bakterii. Po uszkodzeniu ściany następuje pęknięcie i rozpłynięcie się komórki bakterii, czyli tzw. liza, stąd nazwa enzymu. Jego cząsteczka składa się ze 129 aminokwasów.
Lizozym należy do białek które stosunkowo łatwo krystalizują, dlatego wcześnie poznano jego strukturę.
Kryształy na zdjęciach są takie sobie, przede wszystkim bardzo małe, może za parę dni bardziej urosną. Natomiast zachwyciła mnie gra kolorów widoczna pod filtrem polaryzacyjnym. Jestem mimo wszystko trochę estetą.
Tak że teraz zająłem się czymś bliższym chemii fizycznej, czyli badaniami krystalograficznymi. Prawdopodobnie ostateczny temat będzie zawierał cześć syntetyczną i część krystalograficzną. Na razie jednak nadrabiam teorię i praktykę, bo obsługi dyfraktometru rentgenowskiego na studiach nie miałem, przez pierwszy semestr chodzę też na zajęcia specjalizacyjne ze studentami.
Przygotowuję powoli wpis na temat tego krystalografii i tego jak można kryształom zrobić prześwietlenie.
Lizozym to enzym bakteriobójczy, powodujący rozkład glikoprotein w ścianie komórkowej bakterii. Po uszkodzeniu ściany następuje pęknięcie i rozpłynięcie się komórki bakterii, czyli tzw. liza, stąd nazwa enzymu. Jego cząsteczka składa się ze 129 aminokwasów.
Lizozym należy do białek które stosunkowo łatwo krystalizują, dlatego wcześnie poznano jego strukturę.
Kryształy na zdjęciach są takie sobie, przede wszystkim bardzo małe, może za parę dni bardziej urosną. Natomiast zachwyciła mnie gra kolorów widoczna pod filtrem polaryzacyjnym. Jestem mimo wszystko trochę estetą.
* * *
Myślę, że dobrze by było przy tej okazji parę rzeczy objaśnić, bo może regularnie zaglądający zastanawiali się nad paroma kwestiami. Ponieważ prace typowo syntetyczne na pracowni prof. Czarnockiego nie bardzo mi wychodziły, ostatecznie zmieniłem promotora i temat pracy, bo istniało ryzyko, że ciągnąc dotychczasowy mógłbym nie otrzymać wyników na satysfakcjonującą pracę doktorską.Tak że teraz zająłem się czymś bliższym chemii fizycznej, czyli badaniami krystalograficznymi. Prawdopodobnie ostateczny temat będzie zawierał cześć syntetyczną i część krystalograficzną. Na razie jednak nadrabiam teorię i praktykę, bo obsługi dyfraktometru rentgenowskiego na studiach nie miałem, przez pierwszy semestr chodzę też na zajęcia specjalizacyjne ze studentami.
Przygotowuję powoli wpis na temat tego krystalografii i tego jak można kryształom zrobić prześwietlenie.
Subskrybuj:
Posty (Atom)